Гидрид - элемент
Cтраница 3
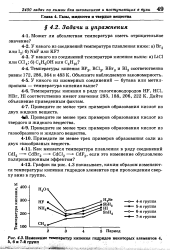 |
Изменение температур кипения гидридов некоторых элементов 4, 5, в и 7 - й групп... [31] |
График на рис. 4.3 показывает, каким образом изменяются температуры кипения гидридов элементов при прохождении сверху вниз в группе. [32]
Оценка частоты инверсии пирамиды, сделанная на основе спектральных данных для гидридов элементов пятой группы [60], а также квантовохимических расчетов для соответствующих триметильных соединений позволяет ожидать, что производные сурьмы типа R3Sb имеют достаточно устойчивую конфигурацию. [33]
В табл. 62 даны ( при температуре кипения) некоторые свойства гидридов элементов главной подгруппы S - й группы. [34]
Фосфин и его алкил -, арилзамещенные, как лиганды, отличаются от гидридов элементов 2-го периода. Фосфины имеют, как свободные акцепторные орбиты для я-электронов, а именно Зс. Фосфины, поэтому, являются весьма сильными основаниями. Фосфины способны стабилизировать как высшие, так и низшие степени окисления переходных металлов. [35]
Имея только один электрон, атом водорода может образовывать одну ковалентную связь; поэтому в гидридах элементов, способных образовывать ковалентные связи ( подгруппы IVA-VIIA), он выступает, как одновалентный. [36]
Объяснить, пользуясь представлениями о строении молекул, как изменяются прочность, восстановительная способность и электрон-но-донорные свойства гидридов элементов главной подгруппы V группы. [37]
Согласно самой общей классификации, по-видимому, первоначально намеченной в работах Смита [16], Шмидта [17] и Хюттига [18], гидриды элементов принято подразделять на три больших класса: летучие гидриды с ковалентной связью; соле-образные с электроотрицательным водородом и так называемые металлические гидриды, к которым относятся преимущественно водородные соединения переходных металлов, включая лантаноиды и актиноиды ( см. таблицу на стр. [38]
Исключения составляют аммиак, вода и фтороводород: температура кипения всех трех веществ намного выше значения, ожидаемого из сравнения с другими гидридами элементов той же группы. Так, например, для воды путем экстраполяции от гидрида серы была предсказана температура кипения - 80 С. [39]
В терминах локализованных орбиталей ( мы всюду используем критерий Бойса) возможна простая систематика корреляционного вклада ПНЭП, что показывают данные табл. 3 [23] для гидридов элементов второго периода. [40]
Следует отметить, что в тех случаях, когда молекула симметрична и результирующий дипольный момент отсутствует, например у метана, температура кипения оказывается низкой даже для гидрида элемента первого ряда. [41]
По этой реакции получаются гидриды всех классов, например, гидриды всех элементов 2-го периода периодической системы, гидриды всех элементов подгрупп IA и VIIA, значительное количество гидридов элементов других групп периодической системы, в том числе гидридов переходных металлов. Реакции протекают при различных температурах и давлении водорода, как с катализаторами, так и без них. Для многих гидридов этот метод получения ( лабораторный или производственный) является главным. Следует отметить, что для некоторых гидридов, например для диборана, установлена только принципиальная возможность осуществления указанной реакции. [42]
Из табл. 1.4 видно, что у гидридов элементов 2-го периода температуры плавления и кипения, а также теплоты испарения меньше отличаются друг от друга, чем в случае гидридов элементов 1-го периода: в наибольшей степени это относится к NH3, H20 и HF. [43]
Среди реакций МОС, продукты которых могут быть применены в электропике, можно отметить три основных типа: 1) реакции МОС с выделением металла, 2) реакции МОС с образованием окислов, нитридов и карбидов, 3) реакции совместного распада двух и более МОС или МОС с гидридами элементов. [44]
 |
Классификация гидридов. [45] |
Страницы: 1 2 3 4