Ионный гидрид
Cтраница 2
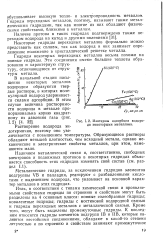 |
Изотермы адсорбции водорода некоторыми металлами. [16] |
Гидриды некоторых переходных металлов весьма похожи на ионные гидриды. Эти соединения имеют большие теплоты образования и характерную структуру, отличающуюся от структуры металла. [17]
Из данных табл. 1.6 видно, что для ионного гидрида лития плотность значительно возрастает по сравнению с литием и соответственно расстояние между центрами атомов уменьшается. Такая же закономерность наблюдается и для других ионных гидридов щелочных и щелочноземельных металлов ( см. гл. [18]
По существу этот метод является новым развитием метода восстановления ионными гидридами с одновременной регенерацией щелочного металла. Сообщается, что при соответствующем избытке SiCU этим путем можно также получить продукты частичного восстановления SiH3Cl, SiHaCb, HSiCl3, что выгодно отличает этот метод от рассмотренного выше. [19]
 |
Свойства гидридов. [20] |
На рис. 17.5 показано в какой части Периодической таблицы расположены элементы, образующие ионные гидриды. [21]
В соответствии с этим, гидриды щелочных и щелочноземельных металлов относятся к группе ионных гидридов. [22]
Ковалентные комплексные гидриды металлов образуют больше стабильных экваториальных спиртов, в то время как ионные гидриды дают больше нестабильных аксиальных спиртов. [23]
Гидриды элементов побочной подгруппы III группы периодической таблицы - лантанидов и актинидов - по своему поведению занимают промежуточное положение между гидридами внедрения и ионными гидридами. Со вторыми они сходны своей значительно более высокой реакционной способностью. [24]
Выведенное выше уравнение для АЯ, видоизмененное соответствующим образом для тех случаев, когда соединение имеет формулу, отличную от MX, позволяет рассмотреть вопрос о стабильности ионных соединений. Вследствие этого ионные гидриды дают только самые электроположительные металлы, для которых член ( ДЯ, АЯ. [25]
Гидриды s - эле-ментов I группы, как и большинство галогенидов этих элементов, имеют структуру типа NaCl. В химическом отношении ионные гидриды ведут себя как основные соединения. [26]
Как показывают приведенные в табл. 35 окислительные потенциалы, ион Н - неустойчив в водном растворе. При растворении в воде ионные гидриды быстро реагируют с ней, образуя Н2 - Они также окисляются на воздухе, хотя обычно не так быстро, как сами исходные металлы. [27]
Гидриды ЭНз построены по типу флюорита ( см. рис. 69, Б) и имеют еолеобразный характер. Они в большей мере напоминают ионные Гидриды гцелочно-земельных металлов, а с гидридами rf - элементов имеют мало общего. Водородные соединения лантаноидов - химически весьма активные вещества, очень энергично взаимодействуют с водой, кислородом, галогенами и другими окислителями. [28]
Гидриды ЭН2 построены по типу флюорита ( см. рис. 70, а) и имеют солеобразный характер. Они в большей мере напоминают ионные гидриды щелочноземельных металлов, а с гидридами d - элементов имеют мало общего. Водородные соединения лантаноидов - химически весьма активные вещества, очень энергично взаимодействуют с водой, кислородом, галогенами и другими окислителями. [29]
 |
Некоторые типы полиэдров, отвечающих характерным координационным числам лантаноидов ( III. [30] |
Страницы: 1 2 3 4