Солеобразный гидрид
Cтраница 1
Солеобразные гидриды водород образует с большинством элементов главных подгрупп I и II групп. В солеобразных гидридах водород является электроотрицательной составной частью ( см. гидрид лития стр. При этом он ведет себя как галоген. [1]
 |
Классификация гидридов. [2] |
Солеобразные гидриды получают прямой реакцией металла с водородом при 300 - 700 С. Они очень легко реагируют с водой и воздухом ( кроме LiH) и все являются мощными восстановителями и гидрирующими агентами. [3]
Солеобразные гидриды при нагревании до высоких температур обратимо разлагаются на металл и водород. Фаза металла способна растворять некоторое количество водорода, а фаза гидрида несколько обедняется водородом. Взаимная растворимость меняется от металла к металлу, но во всех случаях увеличивается при повышении температуры так же, как увеличивается и равновесная упругость водорода над гидридом. [4]
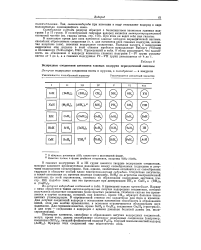 |
Водородные соединения элементов главных подгрупп периодической системы. [5] |
Солеобразные гидриды водород образует с большинством элементов главных подгрупп I и II групп. В солеобразных гидридах водород является электроотрицательной составной частью ( см. гидрид лития, стр. При этом он ведет себя как галоген. [6]
Солеобразные гидриды образуются при непосредственном соединении с водородом щелочных и щелочно-земельных металлов. Водород в солеобразных гидридах формально функционирует как галогены, однако связь здесь имеет менее ионный характер. Тем не менее гидриды щелочных металлов образуют кристаллические структуры типа NaCl - а гидриды щелочно-земельных металлов - более сложные слоистые структуры. [7]
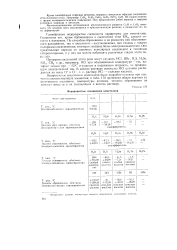
Известные солеобразные гидриды и некоторые их физические свойства приведены в табл. 6.2. Теплоты образования солеобразных гидридов по сравнению с теплотами образования галогенидов щелочных металлов, которые равны примерно 100 ккал / моль, свидетельствуют о невысокой стабильности гидрид-ионов. [8]
Солеобразные гидриды LiH и СаН2 представляют собой кристаллические вещества с ионными решетками, по внешнему виду и физическим свойствам похожие на соответствующие соли галогенов. Однако по химическим свойствам эти соединения сильно отличаются от галогенидов. Солеобразные гидриды - малоустойчивые вещества, являющиеся сильнейшими восстановителями. [9]
Подобно солеобразным гидридам щелочных и щелочноземельных металлов эти гидриды также являются сильными восстановителями. [10]
 |
Водородистые соединения неметаллов. [11] |
Кроме солеобразных гидридов металлов, водород с металлами образует соединения металлического типа. Их нужно отнести к группе интерметаллических соединений. Они представляют собой переход к твердым растворам водорода в металлах. [12]
К солеобразным гидридам относятся также дигидриды бария, стронция, европия, иттербия и магния. [13]
Типичными представителями солеобразных гидридов являются гидриды щелочных и щелочноземельных металлов. Поэтому гидриды указанных металлов очень похожи на соединения металлов с галогенами. [14]
Водород в солеобразных гидридах формально функционирует как галогены, однако связь здесь имеет менее ионный характер. Тем не менее гидриды щелочных металлов образуют кристаллические структуры типа Nad, а гидриды щелочно-земельных металлов - более сложные слоистые структуры. [15]
Страницы: 1 2 3 4