Солеобразный гидрид
Cтраница 2
Какие элементы образуют солеобразные гидриды. Как практически доказать, что водород в них проявляет отрицательную валентность. [16]
По физическим свойствам солеобразные гидриды похожи на соответствующие галоидные соли. [17]
При нагревании все солеобразные гидриды ( кроме LiH, плавящегося при 668 С без разложения) начинают разлагаться на металл и водород еще до достижения точек плавления. Для производных Na-Cs начало заметного распада лежит при 300 - 350 С, для гидридов щелочноземельных металлов - около 600 С. Термическая диссоциация последних сопровождается образованием растворов водорода в выделяю -, щемся металле, что сближает их с гидридами переходного типа. [18]
По физическим свойствам Солеобразные гидриды похожи на соответствующие галоидные соли. [19]
При нагревании все солеобразные гидриды ( кроме LiH, плавящегося при 668 С без разложения) начинают разлагаться на металл и водород еще до достижения точек плавления. Для производных Na - Cs начало заметного распада лежит при 300 - 350 С, для гидридов щелочноземельных металлов - около 600 С. Термическая диссоциация последних сопровождается образованием растворов водорода в выделяющемся металле, что сближает их с гидридами переходного типа. [20]
При нагревании все солеобразные гидриды ( кроме LiH) начинают диссоциировать с - отщеплением водорода до достижения температуры плавления. Выделяющийся при этом водород способен частично растворяться в расплавленном металле. [21]
При нагревании все солеобразные гидриды ( кроме LiH) начинают диссоциировать с отщеплением водорода до достижения температуры плавления. Выделяющийся при этом водород способен частично растворяться в расплавленном металле. Гидрид лития плавится без разложения. [22]
При нагревании все солеобразные гидриды ( кроме LiH плавящегося при 668 С без разложения) начинают разлагаться на металл и водород еще до температуры плавления. Для производных Na - Cs начало заметного распада лежит при 300 - 350 С, для гидридов щелочноземельных металлов - около 600 С. Термическая диссоциация последних сопровождается образованием растворов водорода в металле, что сближает их с гидридами переходного типа. [23]
При нагревании все солеобразные гидриды ( кроме LiH) начинают диссоциировать с отщеплением водорода до достижения температуры плавления. Выделя -, ющийся при этом водород способен частично растворяться в расплавленном металле. [24]
При высокой температуре чистые солеобразные гидриды имеют вполне-определенное давление разложения; частично разложенные препараты LiH, СаН2 или ВаН2 характеризуются значительно меньшим давлением разложения. [25]
С водородом церий образует солеобразные гидриды СеН2 и СеН3, которые являются очень активными восстановителями. [26]
Сильно электроположительные элементы дают чрезвычайно реакционноспособ-ные солеобразные гидриды, например NaH, где водород находится в виде аниона. Между этими крайними случаями находятся твердые полимерные гидриды, причем некоторые из них чрезвычайно реакционно-способны, например А1Н3, и в этом отношении они подобны соле-образным гидридам. В эту схему не укладываются переходные металлы, образующие твердые нестехиометрические гидриды типа сплавов, а также ряд неустойчивых и часто неясно определяемых комплексных гидридов. Подобно тому как переходные металлы не дают устойчивых алкилов типа MRn, они не дают также соответствующих гидридов. Между различными типами гидридов имеется непрерывная, но ясная градация. [27]
Известно несколько методов получения солеобразных гидридов, но наиболее удобным до сих пор считается взаимодействие металла с водородом при повышенных температурах. [28]
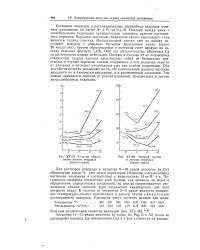 |
Теплоты образования летучих гидридов ( ккал / г-связь. [29] |
Поэтому между ними и солеобразными гидридами принципиально возможно наличие постепенного перехода. Хорошим примером соединения такого переходного типа является гидрид лангана. Металлический лантан уже на холоду поглощает водород с довольно большим выделением тепла ( около 20 ккал / г-экв), причем образующийся в конечном счете продукт по составу отвечает формуле LaHs. Оба эти обстоятельства сближают La со щелочноземельными металлами. Однако, в отличие от их водородных соединений, гидрид лантана представляет собой не бесцветные кристаллы, а черный порошок, причем содержание в нем водорода зависит от давления и начинает уменьшаться уже при слабом нагревании. Оба эти обстоятельства указывают на то, что поглощенный водород частично находится не в химически связанном, а в растворенном состоянии. Тем самым намечается переход от рассматриваемых производных к группе металлообразных гидридов. [30]
Страницы: 1 2 3 4