Гидрирование - органическое соединение
Cтраница 2
Гидрид титана является хоррщим катализатором некоторых реакций гидрирования органических соединений - Он находит использование также в порошковой доета. Термическим разложением обоих гидридов, могут быть получены тонкие, пленки соответствующего металла на различных материалах, что важно для ряда областей техники. [16]
При нанесении платины или палладия на активированный уголь гидрирование органических соединений, в том числе нитросоединений, протекает почти при обратимом водородном потенциале. Это свидетельствует или о значительной концентрации водорода в порах угля, или о преимущественной адсорбции непредельного соединения на поверхности угля с освобождением поверхности платины ( или палладия) для преимущественной адсорбции водорода. Последнее предположение кажется нам боле е вероятным. Подобное же явление встретилось нам при гидрировании диметилацетиленилкарбинола на сплавах палладия с серебром. Скорость реакции на сплавах состава Pd: Ag2: 1 и 1: 1 обратно пропорциональна концентрации карбинола в растворе, падение потенциала довольно значительно и достигает 200 - 250 мв. Таким образом, ацетиленилкарбинол в значительной мере вытесняет водород с поверхности. [17]
В реакциях орто-парапревращения водорода, дейтероводородного обмена, гидрирования органических соединений, изомеризации, гидро-генолиза, в реакции Фишера - Тропша и многих других реакциях с участием водорода применяются нанесенные металлические катализаторы, В некоторых из этих реакций обмен, изомеризация, гидрогено-лиз, активность ( на единицу-поверхности) и избирательность катализатора зависят от формы и дисперсности частиц металла. Чтобы понять механизм таких структурночувствительных реакций, необходимы тщательные эксперименты с применением такого катализатора, в котором кристаллы металла были бы распределены равномерно. В связи с этим интересны также результаты исследования низковалентных металлоорганических комплексов. [18]
Оксидные катализаторы и их смеси широко используют в процессах гидрирования органических соединений ( альдегидов, сложных эфиров, кислот и др.), дегидрирования спиртов и углеводородов ( например, бутана, изопентана, этилбензола), реакциях ва основе оксида углерода при повышенных температурах и давлениях. [19]
Осмий используется в качестве катализатора при синтезе аммиака и гидрировании органических соединений. [20]
Так, при электровосстановлении на металлах с низким перенапряжением водорода часто гидрирование органических соединений происходит под действием водорода, выделяющегося на электроде, а металл нередко играет роль катализатора. На электродах же с высоким перенапряжением обычно происходит перенос электронов на восстанавливающееся вещество, причем в кислых средах переносу электронов часто предшествует протониза-ция органических молекул, значительно облегчающая протекание электрохимической реакции ( см. гл. [21]
 |
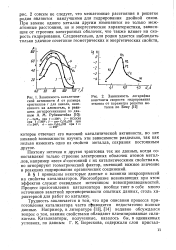
I. Зависимость скорости реакции гидрирования п - нитрофенола от его концентрации при давлении водорода 10 МПа. [22] |
Такая ситуация имеет место, например, в реакциях окисления или гидрирования органических соединений. [23]
Конверсия СО является составной частью процесса производства водорода для синтеза аммиака и гидрирования органических соединений. [24]
Как катализатор, железо может использоваться наряду с обычно применяющимся никелем при гидрировании органических соединений с двойной и тройной связями [ 333, стр. [25]
Металлический никель в мелкораздробленном состоянии при повышении температуры поглощает водород, применяется как катализатор при гидрировании органических соединений. [26]
Коллоидные металлы восьмой группы периодической системы являются одними из первых катализаторов, которые применялись при гидрировании органических соединений. [27]
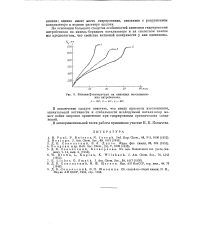 |
Влияние ] температуры на кинетику восстановления нитробензола. [28] |
В заключение следует отметить, что ввиду простоты изготовления, значительной активности и стабильности исследуемый катализатор может найти широкое применение при гидрировании органических соединений. [29]
Страницы: 1 2 3 4