Гидрирование - циклогексен
Cтраница 2
Теплота гидрирования диена почти вдвое больше теплоты гидрирования циклогексена, и, следовательно, теплота гидрирования трех двойных связей в структуре Кекуле, при условии их локализации, должна была бы иметь порядок величины - 28 6 ХЗ - 85 8 ккал / моль. Однако в действительности, как показывает опыт, при гидрировании бензола выделяется только 49 8 ккал / моль. Энергию, на величину которой молекула бензола стабилизована по сравнению с молекулой гипотетического циклогексатриена, имеющего локализованные двойные связи, правильно было бы называть энергией стабилизации. Тем не менее, ее часто называют энергией делокализации, хотя вопрос о том, в какой мере стабилизация действительно обусловлена делокализацией, далеко не ясен. Широко используется также термин энергия резонанса, однако этот термин совершенно неудовлетворителен с семантической точки зрения, поскольку слово резонанс ассоциируется обычно с быстрыми переходами, осцилляциями между различными структурами ( например, в случае бензола - между структурами Кекуле), которых в действительности нет. [16]
Теплота гидрирования диена почти вдвое больше теплоты гидрирования циклогексена, и, следовательно, теплота гидрирования трех двойных связей в структуре Кекуле, при условии ЕХ локализации, должна была бы иметь порядок величины - 28 6 X 3 - 85 8 ккал / моль. Однако в действительности, как показывает опыт, при гидрировании бензола выделяется только 49 8 ккал / моль. Энергию, на величину которой молекула бензола стабилизована по сравнению с молекулой гипотетического циклогексатриена, имеющего локализованные двойные связи, правильно было бы называть энергией стабилизации. Тем не менее, ее часто называют энергией делокализации, хотя вопрос о том, в какой мере стабилизация действительно обусловлена делокализацией, далеко не ясен. Широко используется также термин энергия резонанса, однако этот термин совершенно неудовлетворителен с семантической точки зрения, поскольку слово резонанс ассоциируется обычно с быстрыми переходами, осцилляциями между различными структурами ( например, в случае бензола - между структурами Кекуле), которых в действительности нет. [17]
Влияние первого фактора удобно показать на примере гидрирования циклогексена или замещенных олефинов. Для подобных соединений энергия связи водорода с поверхностью катализатора настолько велика, что поверхность катализатора, покрытая водородом, не взаимодействует с непредельным соединением. На этих катализаторах циклогексен хорошо гидрируется в спиртовой или спиртовокислой среде уже при комнатной температуре. Подкисление раствора полностью восстанавливает активность катализатора. КОН гидрирование гексена полностью прекращается. Наблюдаемый эффект обусловлен тем, что водород, легко снимаемый с катализатора олефином в спиртовом растворе, становится нереакционно-способным при подщелачивании раствора вследствие упрочнения энергии связи водорода с поверхностью катализатора. [18]
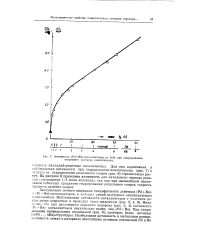 |
Активность ( Рс1 КЬ-катадизаторов на SiO2 при гидрировании спиртового раствора циклогексена. [19] |
Для них аддитивная и наблюдаемая активности при гидрировании циклогексена ( рис. 7) в отличие от гидрирования аллилового спирта ( рис. 8) стремительно растут. На рисунке 8 приведена активность для начального периода реак-шш ( поглощение 1 / 3 моля водорода), так как при дальнейшем накоплении побочных продуктов гидрирования аллилового спирта скорость процесса заметно падает. [20]
Отправной точкой в таком подсчете является значение теплоты гидрирования циклогексена. [21]
 |
Схематическое изображение двенад-цатиатомного платинового ансамбля. [22] |
На рис. 6 представлена относительная величина активности центров гидрирования циклогексена и 1-гептена. За единицу принята активность двухатомного платинового ансамбля, адсорбированного на силика-геле. Как видно из рис. 6, при усложнении гидрогейизационного центра циклогексен как бы обгоняет 1-гептен по скорости гидрирования. [23]
Активность разбавленных слоев палладий-иридиевых адсорбционных катализаторов в реакциях гидрирования циклогексена, аллилового спирта и разложения перекиси водорода / / Физ. [24]
Исследовано [42] влияние размеров металлических кластеров на скорость гидрирования циклогексена и бензола в присутствии Pt-и Pt-Au - катализаторов. [25]
Так, исходя из того, что теплота гидрирования циклогексена составляет 28 6 ккал / моль, можно предположить, что гипотетические структуры 1 и 2 с тремя двойными связями должны иметь теплоту гидрирования около 85 8 ккал / моль. Теплота гидрирования реальной молекулы бензола равна 49 8 ккал / моль, отсюда энергия резонанса составляет 36 ккал / моль. [26]
Таким образом, изучение влияния состава растворителя на скорость гидрирования циклогексена на Pt-Pd и никелевом катализаторе при -, водит к выводу о решающей роли в этом случае энергии связи водорода с поверхностью и скорости его активации. [27]
Для измерений парахора Фогель [1936] ПОЛУЧИЛ с хорошим выходом циклогексан гидрированием циклогексена в присутствии катализатора Адамса [ 709, стр. [28]
В качестве примера гидрирования на компактном катализаторе рассмотрим наши данные по гидрированию циклогексена на платиновой черни, отравленной сулемой. Соответствующий график приведен на рис. 6, в. В табл. 5 приведены расчеты величины vh для различных образцов Pt-черней. [29]
Известно [34], что Pi - и Pd-катализаторы обладают различной стереоселективностью при гидрировании циклогексенов. На Pt-катализаторе в растворе уксусной кислоты продуктами гидрирования являются главным образом ч с-изомеры, а на Pd - транс-изомеры. С точки зрения Го, Руни и Кемболла [15], эти факты могут быть объяснены разной способностью этих металлов образовывать я-аллильные промежуточные комплексы. [30]
Страницы: 1 2 3 4