Гидрирование - циклогексен
Cтраница 3
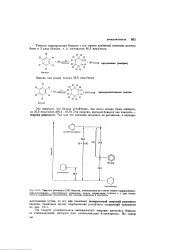 |
Энергия резонанса ( ЭР бензола, вычисленная на основе теплот гидрирования. [31] |
Циклогеисатриен - гипотетическое соединение, теплота гидрирования которого в 3 раза больше теплоты гидрирования циклогексена. [32]
Наибольшее отравляющее действие кадмий оказывал при гидрировании ароматической связи, меньшее - при гидрировании циклогексена. Циклогексен при 130 С гидрировался на 99 % при содержании 2 % Cd; олефины гидрируются еще лучше. [33]
Теплота реакции I - - II равна - 25 6 ккал, что несколько меньше теплоты гидрирования циклогексена, равной - 27 1 ккал. Это указывает на некоторую стабилизацию циклооктатетраена. [34]
При гидрировании бензола выделяется около 208 кДж / моль ( теплота гидрирования), а при гидрировании циклогексена - 120 кДж / моль. Разница в теплотах гидрирования трех изолированных двойных связей и бензола составляет 3 - 120 - 208152 кДж / моль. Из этого можно сделать вывод, что молекула бензола имеет энергию стабилизации около 150 кДж / моль ( ср. [35]
Для каждой каталитической системы, состоящей из триэтилалюминия и соединений титана, никеля или кобальта, при гидрировании циклогексена наблюдается определенный оптимум, зависящий от валентности переходного металла и лигандов, координированных с переходным металлом. [36]
Проведено потснциометрическое исследование бинарных металлических адсорбционных катализаторов на основе палладия и варьируемых компонентов иридия и осмия в реакциях гидрирования циклогексена и аллилового спирта. [37]
Как видно из приведенных уравнений, при гидрировании цикло-гексадиена-1 3 до циклогексена выделяется меньше тепла, чем при гидрировании циклогексена, так как в первом случае в молекуле имеется система сопряженных связей. [38]
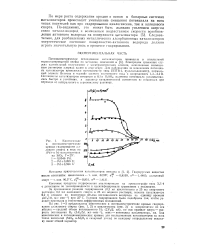 |
Кинетические и потенциометрические кривые гидрирования ал-ливого спирта в воде на ( Рй п 1г - катализаторах. [39] |
По мере роста содержания иридия и осмия в бинарных системах катализаторов происходит уменьшение смещения потенциала на всех типах носителей как при гидрировании циклогексена, так и аллилового спирта. [40]
Установлено небольшое анодное смещение потенциала на 20 - 50 мВ при гидрировании аллилового спирта и до 60 мВ, после поглоще-ния / з моля Н2, при гидрировании циклогексена для обеих систем катализаторов на различных носителях. [41]
Установлено небольшое анодное смещение потенциала на 20 - 50 мВ при гидрировании аллилового спирта и до 60 мВ, после поглощения / з моля Н2, при гидрировании циклогексена для обеих систем катализаторов на различных носителях. [42]
Корректность этих выводов проверяем на логарифмической диаграмме; линейная зависимость получается и для трехатомного центра при разложении перекиси водорода, и для двухатомного - при гидрировании циклогексана, и для шестиатомного - при гидрировании циклогексена и бензальанили на, а практическая параллельность прямых, дающая совпадающие между собой значения ZQ, указывает на правильность расчета этой величины из первого максимума активности для разложения перекиси водорода. Существуют и другие методы расчета состава сложных активных центров по положению максимумов поли-экстремальных кривых активности. [43]
Кобальтовый катализатор [ ( МеО) зР ] зСо ( г) 3 - С3Н5) обнаруживает интересную селективность, позволяя гидрировать арены в циклогексаны; скорость этой реакции в несколько раз выше, чем скорость гидрирования циклогексенов. Очевидно, что с момента первого переноса водорода и до отщепления циклогексана молекула субстрата остается связанной с атомом металла. [44]
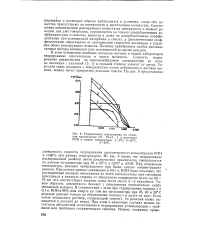 |
Гидрирование циклогексена на сплавном катализаторе Pd. Pt3. 1, в растворах КОН в спирте. температура. / - 9 С. 2 - 25 С. 3 - 50 С. [45] |
Страницы: 1 2 3 4