Гидроксид - железо
Cтраница 1
Гидроксид железа ( II), образованный сначала замещением серы в кристаллической решетке пирита анионами ОН -, метаста-бялен. Он распадается на гексагональные уплотненные конфигурации, имеющие вид мелкозернистого материала, с появлением которого связано замедление реакции разложения пирита. [1]
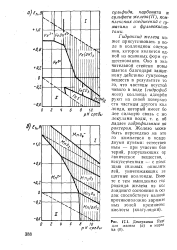 |
Диаграммы Пур для железа ( а и марга ца ( б. [2] |
Гидроксид железа может присутствовать в воде в коллоидном состоянии, которое является одной из основных форм существования. Железо може быть переведено из это го комплекса в осадо двумя путями: естествен ным - при участии бак терий, разрушающих ор ганическое вещество, , искусственным - с помс щью сильных окислите лей, уничтожающих за щитные коллоиды. [3]
Гидроксиды железа из воды наиболее эффективно извлекаются в осветлителях со слоем взвешенной контактной среды. Благодаря гетерогенно-каталитическому процессу железо ( II) в слое взвешенной контактной среды окисляется быстрее. На эффект обезжелезивания влияют рН; температура, исходная концентрация железа, высота слоя осадка и скорость восходящего потока воды. [4]
Гидроксид железа ( III) образуется при взаимодействии хлорида железа ( III) с карбонатом аммония. С этой целью 2 мл насыщенного ( без нагревания) хлорида железа ( III) разбавляют водой до 50 мл. При энергичном взбалтывании в раствор вводят каплями 20 % - ный раствор ( МН СОз до тех пор, пока выпадающий гидроксид железа ( III) перестает растворяться при взбалтывании. Для его пептизации прибавляют несколько капель насыщенного раствора РеСЬ и сильно встряхивают колбу с раствором до полного исчезновения осадка. [5]
Гидроксид железа ( П) Fe ( OH) 2 выпадает из водных растворов солей железа ( П) при добавлении щелочей. В избытке раствора щелочей гидр-оксиды железа практически не растворяются. [6]
Гидроксид железа ( III) Fe ( OH) 8 имеет практически основной характер. [7]
Гидроксид железа ( III) - более слабое основание, чем гидроксид железа ( II); это выражается в том, что соли железа ( III) сильно гидролизуются, а со слабыми кислотами ( например, с угольной, сероводородной) Fe ( OH) 3 солей не образует. [8]
Гидроксид железа ( Ш) - более слабое основание, чем гидроксид железа ( П); это выражается в том, что соли железа ( Ш) сильно гидролизуются, а со слабыми кислотами ( например, с угольной, сероводородной) Ре ( ОН) 3 солей не образует. [9]
Гидроксид железа ( III) - более слабое основание, чем гидроксид железа ( II); это выражается в том, что соли железа ( III) сильно гидролизуются, а со слабыми кислотами ( например, с угольной, сероводородной) Fe ( OH) 3 солей не образует. [10]
Гидроксид железа ( III) - более слабое основание, чем гидроксид железа ( II); это выражается в том, что соли железа ( III) сильно гидролизуются, а со слабыми кислотами ( например, с угольной, сероводородной) Ре ( ОН) 3 солей не образует. [11]
Гидроксид железа ( II) амфотерен, частично растворяется в сильнощелочных средах. [12]
Гидроксид железа ( II) легко растворяется в кислотах. [13]
Гидроксид железа ( III) проявляет основные свойства, растворяется в кислотах. [14]
Гидроксиды железа ( II), кобальта ( И) и никеля ( II) нерастворимы в воде, хорошо растворимы в кислотах, так как обладают слабыми основными свойствами. На воздухе белый Fe ( OH) 2 легко окисляется до красно-коричневого Ре ( ОН) з; окисление же Со ( ОН) 2 ( розового цвета) кислородом воздуха до Со ( ОН) з ( коричнево-бурого) протекает сравнительно медленно. ОН) з - светло-зеленого цвета, устойчив на воздухе. Окисление до № ( ОН) з ( черного цвета) может происходить под действием сильных окислителей, например хлора. [15]
Страницы: 1 2 3 4