Гидроксилы
Cтраница 2
Группы, содержащие гидроксилы, легко вступают в реакцию с мочевиной и другими аналогичными соединениями. Они также взаимодействуют с группами ОН целлюлозного волокна. В результате получаются макромолекулы, содержащие атомы фосфора в качестве существенного элемента их структуры и химически связанные с молекулами целлюлозы; очевидно, что такое покрытие не будет удаляться при стирке. [16]
Двухатомные спирты, гидроксилы которых находятся у двух соседних атомов углерода, рассматривают как производные простейшего двухатомного спирта - эти лен гликоля. [17]
Двухатомные спирты, гидроксилы которых находятся у двух соседних атомов углерода, рассматривают как производные простейшего двухатомного спирта - этиленгликоля. [18]
Обмен галоидов на гидроксилы в галоидных производных альдегидов и кетонов. [19]
Как легко замещаются гидроксилы в первичных, вторичных и третичных спиртах жирного ряда. Сравнить подвижность гидроксилов в спиртах жирного ряда с реакцион-носпособностью гидроксила непредельного ( аллилового) и ароматического ( бензилового) спиртов. [20]
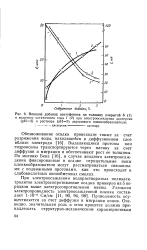 |
Влияние добавок анетофенона на толщину покрытий 6 ( 1. [21] |
Выделяющиеся протоны или гидроксилы транспортируются через пленку за счет диффузии и миграции и обеспечивают рост ее толщины. По мнению Бека [16], в случае анодного электроосаждения фиксированные в осадке отрицательные ионы пленкообразователя могут рассматриваться связанными с подвижными протонами, как это происходит в слабокислотных ионообменных смолах. [22]
 |
Конформация 1 2-диолов с большими циклами. [23] |
В тракс-циклопентандиоле-1 2 гидроксилы слишком отдалены друг от друга для того, чтобы образовать водородную связь. В циклах, содержащих от шести до девяти атомов, г ис-диолы имеют более сильную водородную связь, чем транс-диолы. Это показывает, что с-группы легче пригнуть друг к другу, чем трансгруппы. [24]
Таким образом, гидроксилы оказываются в положениях 1 6, а не в соседних положениях, как этого следовало бы ожидать, исходя из классических представлений. [25]
Гликопиранозильный остаток, гидроксилы которого защищены от окисления ацетилированием, при обработке хромовым ангидридом в уксусной кислоте претерпевает окисление, при котором гликозидная связь превращается в сложнозфирную. Остаток моносахарида превращается при этом в остаток кетоальдоновой кислоты. В эту реакцию вступают только гликозильные остатки, у которых водород при гликозидном центре аксиален ( см. схему на с. Поэтому из двух возможных аномеров моносахаридного остатка внутри полисахариднои цепи окислению подвергается только один. [26]
Гликоли, у которых гидроксилы находятся при соседних атомах углерода, могут быть получены осторожным окислением этиленовых углеводородов ( стр. [27]
Галоидоспиртами, у которых гидроксилы и атомы галоида находятся у разных атомов углерода, являются галоидгидрины многоатомных спиртов ( стр. Благодаря наличию галоида и гидроксильной группы галоидгидрины обладают типическими химическими свойствами как галоидных алкилов, так и насыщенных спиртов. [28]
В конформации 3В все гидроксилы, в том числе и глкжозидный, экваториальны, в конформации В1 гидроксил у второго углеродного ато. [29]
В конформации 3В все гидроксилы, в том числе и глкжозидный, экваториальны, в конформации В1 гидроксил у второго углеродного атома аксиален. [30]
Страницы: 1 2 3 4