Гидроксилы
Cтраница 3
Значительное их число через гидроксилы у С-2 и С-3 соединены с остатками арабинозы и глюкуроновой или 4 - О-метилглюкуроновой кислот. [31]
Если в растворе присутствуют свободные гидроксилы, то давление паров СО2 над раствором настолько мало, что им в большинстве случаев можно пренебречь. [32]
Нитратные группы, замещающие вторичные гидроксилы, с иодом не реагируют. Указанное обстоятельство дает возможность оценить химическую неоднородность нитрата целлюлозы в глюкозных остатках. [33]
G-3 легче ацетилируется, чем гидроксилы при С-17 и С-12. Экваториально ориентированные гидроксильные группы пространственно менее экранированы, чем аксиальные, поэтому и легче ацетилируются ( стр. Только гидроксил при С-3 холевой кислоты занимает экваториальное положение. Гидроксил при С-7 имеет сильно выраженные пространственные препятствия, поскольку вследствие гшс-сочленения циклов А и В одна из метиленовых групп цикла А расположена аксиально и в г / мс-положе-нии к этой функции. [34]
В этой реакции могут участвовать гидроксилы в а - или р-положениях, что приводит к образованию различных изомеров, содержащих 4 гидроксильные группы в случае диглицери-на и 5-в случае триглицерина. Действительно, можно показать наличие полиглицериновых - спиртов в процессе приготовления моноглицеридов. В противоположность предыдущим случаям, в результате реакции не теряется эквивалентное количество глицерина, поскольку функциональность вновь образующихся соединений выше, чем у глицерина. Однако в случае неправильного дозирования фталевого ангидрида эти реакции влияют на качество конечной смолы. [35]
С-3 легче ацетилируется, чем гидроксилы при G-17 и С-12. Экваториально ориентированные гидроксильные группы пространственно менее экранированы, чем аксиальные, поэтому и легче ацетилируются ( стр. Только гидроксил при С-3 холевой кислоты занимает экваториальное положение. Гидроксил при С-7 имеет сильно выраженные пространственные препятствия, поскольку вследствие гfмc - coчлeнeния циклов А и В одна из метиленовых групп цикла А расположена аксиально и в цмс-положе-нии к этой функции. [36]
При действии РС15или НС1 на гидроксилы, непосредственно связанные с асимметрическим атомом, имеет место оптическая инверсия. Ввиду этого создаются условия, благоприятствующие, при отнятии элементов НС1, образованию структурных изомеров. [37]
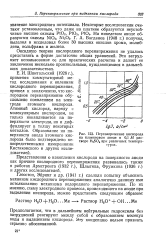 |
Перенапряжение кислорода на платиновом аноде в 0 1 М рас. [38] |
Предполагается, что в дальнейшем нейтральные гидроксилы без затруднений реагируют между собой с образованием молекул воды и выделением кислорода. Эту концепцию нельзя признать серьезно обоснованной. [39]
Реакционноспособными в новолачных смолах являются феноль-ные гидроксилы и атомы водорода бензольного ядра, находящиеся в орто - и пара-положениях. Смолы отверждаются в результате замещения атомов водорода бензольных ядер метиленовыми группами, образующимися при распаде отвердителей - гексаметилен-тетрамина, реже - параформа. [40]
Алкоксильные группы в оксипропнлцеллюлозе содержат вторичные гидроксилы, которые могут взаимодействовать с окисью пропилена. Почти все первичные гидроксильные группы макромолекул целлюлозы замещаются при синтезе этого эфира. Низкозамещенные препараты оксипропилцеллюлозы не растворяются ни в воде, ни в щелочи; только при достижении значения МЗ, близкого к 4, Окснпропилцеллюлоза начинает растворяться в указанных растворителях. Растворимость полиоксипропиленовых цепей понижается при увеличении температуры, и их выделение из водного раствора происходит около 40 С. Аналогичное явление имеет место и в органических растворителях. Получают также препараты оксипропилцеллюлозы, растворимые только в воде. Другие типы этого эфира растворяются как в воде, так и в этаноле. Они растворяются также и в других органических растворителях: низших спиртах, гликолях, хлорсодержащих алифатических и циклических простых эфирах, но плохо растворяются в высших спиртах, циклоалканах, сложных эфирах. [41]
Авторы [176] считают, что гидроксилы кластеров ( ОН) 4 могут сохраняться в деалюминированных цеолитах при температуре даже выше 600 С. [42]
Положительным мезомерным эффектом обладает и гидроксилы пая группа. Свободная электронная пара атома кислорода ОН-группы фенола вступает в сопряжение с ароматическим ядром и с орго-пара-положениях создается повышенная электронная плот-кость, подобно тому как это происходит в анилине. [43]
Так как в них все свободные гидроксилы соединены с метальными группами, то они не могут переходить в циклическую форму и благодаря этому пригодны для изучения свойств альдегидной группы молекул моносахаридов. Со спиртом они легко образуют диэтилацетали. [44]
Удивительно однако то, что флороглюциновые гидроксилы в молекуле антоцианидина с Fe - повидимому не реагируют. Наоборот, цианидин и дельфинидин реагируют весьма интенсивно, окрашиваясь в спиртовом растворе в синий цвет. Диметилдельфинидин ( энидин, или сирингидин) также не реагирует. Таким образом необходимым условием для цветной реакции с Ре - - ( синее окрашивание) является присутствие в молекуле антоциана двух соседних гидроксилов в а-фенилыюм остатке ( см. стр. [45]
Страницы: 1 2 3 4