Спиртовые гидроксилы
Cтраница 2
Полуацетальный гидроксил подвергается ацилировапию производными карбоновых кислот в тех же условиях, что и спиртовые гидроксилы Сахаров. Эта реакция, приводящая в случае свободных моносахаридов к сполна ацилированным производным, рассматривалась в гл. Для синтеза соответствующих производных более сложных карбоновых кислот обычно прибегают к конденсации ацилированных гликозилгалогенидов с солями этих кислот. Тот же прием применяется для синтеза эфиров фосфорной, азотной и некоторых других кислот. Эти реакции аналогичны синтезу арилгликозидов и будут подробнее рассматриваться ниже. [16]
Для лигнина характерны следующие функциональные группы [4]: - ОСН3, фенольные гидроксилы, первичные и вторичные спиртовые гидроксилы, особенно бензилспиртовые, карбонильные, карбоксильные группы. [17]
Макромолекулы эпоксидной смолы способны соединяться с диизоцианатами с образованием полимеров трехмерной структуры, причем в реакции участвуют спиртовые гидроксилы или эпоксидные группы. [18]
Повядимому, ацетшшров энный у азота остаток хондрозина является основной структурной единицей хондроитинсерной кислоты; остатками серной кислоты, как предполагают, этерифи-циро-ваны первичные спиртовые гидроксилы в остатках аминогалактозы. [19]
При метилировании биозы типа трегалозы или сахарозы ( тип гли-козидогликозидный) оба моносахарида имеют после гидролиза по четыре метила, чем еще раз доказывается, что спиртовые гидроксилы не участвовали в связывании моноз в биозу и что эта связь осуществлялась за счет обоих гликозидных гидроксилов. [20]
Для гликозилирования более сложных спиртов или фенолов необходимы методы, предусматривающие применение в качестве гликозилирую-щих агентов таких производных Сахаров, в которых размер цикла жестко фиксирован, а все спиртовые гидроксилы защищены подходящими группами. В настоящее время известно несколько методов, отвечающих этому требованию. [21]
В фенолформальдегидной ( резольной) смоле, со строением которой мы подробно познакомимся позже, имеются гидроксиль-ные группы, связанные с углеродом ароматического кольца ( фенольные гидроксилы), и гидроксильные группы, связанные с углеродом, расположенным вне кольца ( спиртовые гидроксилы), Последние отличаются большей склонностью к реакции поликонденсации, и поэтому они вступают во взаимодействие с такими же гидроксильными группами, оставшимися в поливинилаце-талевой смоле. [22]
Прежде всего была исследована адсорбция гипана - реагента, содержащего преимущественно карбоксильные функциональные группы, - амидных групп и УЩР, функциональные группы которого представлены карбоксильными группами и фенольными гидроксилами, а также лигносульфонатов ( ССБ и окзил), в состав которых входят сульфоновые группы и спиртовые гидроксилы. [23]
В нейтральной среде окисление альдегидной группы альдоз в карбоксильную группу осуществляют действием бромной воды. Спиртовые гидроксилы при этом не затрагиваются. Из D-глюкозы образуется D-глюконовая кислота, кальциевая соль которой, г л ю-конат кальция, используется в медицине. [24]
Гликозидный гидроксил легко взаимодействует даже с метиловым спиртом в присутствии хлористого водорода. Спиртовые гидроксилы в этих условиях не затрагиваются; для их алки-лирования необходимы более сильные алкилирующие агенты, например галогеналкилы ( в присутствии окиси серебра, см. стр. [25]
Среди продуктов конденсации фенола с формальдегидом в указанных условиях и соотношениях главную массу составляют соединения с большим количеством метилольных групп. Соединения, содержащие спиртовые гидроксилы, замедляют, а в большом количестве и вовсе прекращают реакцию между начальными продуктами взаимодействия фенола с формальдегидом. Так, например, хорошо известно замедляющее действие на реакцию фенолальдегидной конденсации этилового спирта, которым часто пользуются в производственных условиях. [26]
Ангидриды Сахаров могут быть получены по общему методу получения гликозидов, но без прибавления спирта - при нагревании са-харов с разбавленными кислотами. Хотя в принципе все спиртовые гидроксилы могут реагировать с полуацетальным, давая разнообразные ангидриды, практически наиболее стабильны лишь 1 6-ангидриды. [27]
Гидроксил, возникший при переходе в циклическую форму у С-1, существенно отличается от остальных гидроксильных групп. В то время как при атомах С-2-С-6 стоят обычные спиртовые гидроксилы, при С-1 гидроксильная группа входит в состав группировки, называемой полу ацеталь ной ( стр. [28]
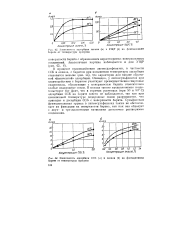 |
Зависимость адсорбции гипана ( о и УЩР ( б на флотационном барите от температуры прогрева.| Зависимость адсорбции ССБ ( а и окяила ( б на флотационном барите от температуры прогрева. [29] |
В процессе взаимодействия лигносульфонатов, в частности ССБ и окзила, с баритом при повышении температуры адсорбция становится меньше ( рис. 44), что характерно для вполне обратимой физической адсорбции. Очевидно, у лигносульфонатов при взаимодействии с баритом участвуют преимущественно спиртовые гидроксилы, образующие с поверхностью барита относительно слабые водородные связи. В пользу такого предположения свидетельствует тот факт, что в горячих растворах ( при 50 и 80 С) адсорбции ССБ на барите совсем не наблюдается, так как при повышенной температуре водородные связи разрушаются, что приводит к десорбции ССБ с поверхности барита. Сульфоновая функциональная группа в лигносульфонатах также не обеспечивает их фиксации на поверхности барита, так как она образует с двух - и трехвалентными катионами достаточно растворимые соединения. [30]
Страницы: 1 2 3