Гидролиз - соль - слабое основание
Cтраница 1
Гидролиз соли слабого основания и слабой кислоты сводится к одновременному гидролизу катиона и аниона такой соли. [1]
Константа гидролиза соли слабого основания и сильной кислоты равна отношению ионного произведения воды к константе диссоциации слабого основания. [2]
Вследствие сильного гидролиза соли слабого основания и очень слабой кислоты, который идет даже в присутствии избытка кислоты, в этом случае нельзя пользоваться слабым основанием для кондуктометрического определения конечной точки титрования. [3]
В результате гидролиза солей слабого основания и сильной кислоты раствор приобретает кислую реакцию. Чем меньше константа диссоциации основания, тем сильнее равновесие гидролиза соли этого основания смещено вправо. [4]
Аналогично константа гидролиза соли слабого основания и сильной кислоты выражается отношением ионного произведения воды и константы ионизации соответствующего основания. [5]
В результате гидролиза солей многокислотных слабых оснований образуются основные соли. [6]
Аналогично, константа гидролиза соли слабого основания и сильной кислоты выражается отношением ионного произведения воды и константы ионизации соответствующего основания. [7]
Отсюда видно, что степень гидролиза соли слабого основания и слабой кислоты не зависит от разбавления раствора. [8]
Аналогичное соотношение получается для случая гидролиза соли слабого основания и сильной кислоты. [9]
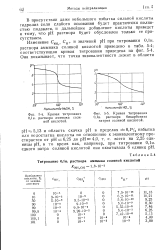 |
Титрование 0 1 н. раствора аммиака соляной кислотой. [10] |
В присутствии даже небольшого избытка сильной кислоты гидролиз соли слабого основания будет практически полностью подавлен, и дальнейшее добавление кислоты приведет к тому, что рН раствора будет обусловлен только ее присутствием. [11]
Из последнего уравнения видно, что степень гидролиза соли слабого основания и слабой кислоты, когда / СЛ10Н - НА от концентрации соли зависит в малой степени, лишь через посредство коэффициента активности. [12]
Из последнего уравнения видно, что степень гидролиза соли слабого основания и слабой кислоты, когда Кмон Л НАН, от концентрации соли зависит в очень незначительной степени. Эта зависимость сказывается только в связи с изменением ионной силы раствора и как следствие коэффициента активности. [13]
Таким образом, концентрация водородных ионов при гидролизе соли слабого основания и слабой кислоты не зависит от разведения, а зависит только от констант диссоциации кислоты и основания. [14]
Так как подвижности водородных ионов, получающихся при гидролизе солей слабых оснований, выше подвиж-постей гидроксильных ионов, образующихся при гидролизе солей слабых кислот, то наблюдается более резкое понижение электропроводности раствора до точки эквивалентности при титровании солей, подвергающихся сильному гидролизу. Минимум на кривых титрования солей слабых оснований, наблюдающихся в случаях, когда степень гидролиза солей равна нескольким процентам, более глубокий, чем при титровании солей, образованных катионами слабых оснований такой же силы. [15]
Страницы: 1 2 3