Гидролиз - соль - слабое основание
Cтраница 2
Эти уравнения, однако, не применимы для расчета гидролиза солей слабых оснований и слабых кислот. В этом случае следует учитывать все уравнения от ( 2) до ( 6), и тогда не получается пр остого соотношения между концентрацией водородных ионов и степенью гидролиза. [16]
Эти уравнения, однако, не применимы Щя расчета гидролиза солей слабых оснований и слабых кислот. В этом случае следует учитывать все уравнения от ( 2) до ( 6), и тогда не получается простого соотношения между концентрацией водородных ионов и степенью гидролиза. [17]
Из реакций (6.19) - (6.21) ясно, что в результате гидролиза солей слабого основания и сильной кислоты раствор приобретает кислую реакцию. [18]
Из приведенных примеров видно, что обычные реакции электролитической диссоциации ( I), гидролиза солей слабых оснований ( II) и солей слабых кислот ( III), а также нейтрализации ( IV) - все представляют собой частные случаи протолитических реакций взаимодействия кислот и оснований, понимаемых в общем виде. [19]
Из рассмотрения реакций ( 7) - ( 9) ясно, что в результате гидролиза солей слабого основания и сильной кислоты образующийся раствор проявляет кислую реакцию. [20]
Поскольку оснований и кислот с одинаковыми по величине константами диссоциации существует очень мало, необходимо тщательно изучить гидролиз соли слабого основания и слабой кислоты для случая, когда Квон ф КНА. [21]
Из выражений ( IV, 19), ( IV20) и ( IV21) видно, что при гидролизе соли слабого основания и слабой кислоты степень гидролиза не зависит в первом приближении от общей концентрации соли. [22]
В этом равновесии Н и ОН - - ионы не участвуют, тогда как в уравнении ( 7 7), которое описывает гидролиз соли слабого основания и сильной кислоты, фигурируют Н - ИОНЫ, а в схемах, изображающих гидролиз солей сильных оснований и слабых кислот, обязательно появляются ОН - - ионы. Одновременное отсутствие Н и ОН - - ионов в уравнении ( 7 22) вполне правомерно, если Квон - КНА, так как в этом случае они появляются и исчезают в равных количествах, благодаря чему равновесный раствор даже сильно гидролизованной соли сохраняет нейтральную реакцию. [23]
Из выражений ( IV, 19), ( IV, 20) и ( IV, 21) видно, что при гидролизе соли слабого основания и слабой кислоты степень гидролиза не зависит в первом приближении от общей концентрации соли. [24]
Анализ уравнений (4.19), (4.20) и (4.24) показывает, что степень гидролиза солей слабых кислот и сильных оснований и сильных кислот и слабых оснований уменьшается с ростом концентрации соли и, следовательно, увеличивается при разбавлении растворов; степень гидролиза солей слабого основания и слабой кислоты от концентрации раствора практически не зависит. [25]
Из уравнения ( 22) ясно, что количественная сторона степени гидролиза соли слабой кислоты и сильного основания должна быть определена величиною константы ионизации кислоты и ионным произведением воды. Соответственно гидролиз соли слабого основания и сильной кислоты определяется константой ионизации основания и ионным произведением воды, и задача вычисления концентрации водородных ионов в таких гидролизованных растворах солей не представляет затруднения. [26]
Степень гидролиза соли зависит от следующих факторов: 1) от константы диссоциации кислоты или основания, образующихся в процессе гидролиза; чем она меньше, тем больше степень гидролиза; 2) от температуры; при нагревании раствора гидролиз усиливается, так как увеличивается степень диссоциации воды, становятся больше [ Н ] и [ ОН - ]; 3) для солей, образованных сильными кислотами и слабыми основаниями, а также сильными основаниями и слабыми кислотами, степень гидролиза возрастает при разбавлении раствора. Степень гидролиза солей слабых оснований и слабых кислот от концентрации соли практически не зависит. [27]
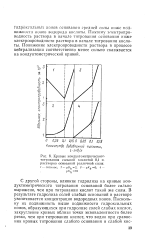 |
Кривые кондуктометрического титрования сильной кислотой 0 1 и. растворов оснований различной силы. / - сильное. 2 - рКь2. 3 - рКь 6. Л. [28] |
С другой стороны, влияние гидролиза на кривые кондуктометрического титрования оснований более сильно выражено, чем при титровании кислот такой же силы. В результате гидролиза солей слабых оснований в растворе увеличивается концентрация водородных ионов. [29]
В теории Бренстеда этот процесс рассматривается как ионизация кислоты МЩ, по природе, не отличающийся от аналогичной ионизации любой другой кислоты, скажем, уксусной. По классическим представлениям этот процесс рассматривается как гидролиз соли слабого основания. [30]
Страницы: 1 2 3