Гидролиз - хлор
Cтраница 1
Гидролиз хлора является реакцией самоокисления-самовосстановления, при которой один из атомов хлора, присоединяя к себе электрон от другого атома, восстанавливается, а другой атом хлора окисляется. [1]
Гидролиз хлора был впервые изучен А. А. Яковкиным ( 1863 - 1936), определившим константу равновесия этой реакции и степень гидролиза хлора при различных температурах. [2]
Гидролиз хлора является реакцией самоокисления-самовосстановления, при которой один из атомов хлора, присоединяя к себе электрон от другого атома, восстанавливается, а другой атом хлора окисляется. [3]
Гидролиз хлора является обратимой химической реакцией самоокисления - самовосстановления, при которой один из атомов хлора присоединяет электрон от другого атома и восстанавливается. [4]
Гидролиз хлора является реакцией самоокисления-самовосстановления, при которой один из атомов хлора, присоединяя к себе электрон от другого атома, восстанавливается, а другой атом хлора окисляется. [5]
Гидролиз хлора является реакцией самоокисления-само восста-новления, при которой один из атомов хлора, присоединяя к себе электрон от другого атома, восстанавливается, а другой атом хлора окисляется. [6]
Гидролиз хлора является реакцией самоокисления-самовосстановления, при которой один из атомов хлора, присоединяя к себе электрон от другого атома, восстанавливается, а другой атом хлора окисляется. [7]
Гидролиз хлора является реакцией самоокисления-самовосстановления, нри которой один из атомов хлора, присоединяя к себе электрон от другого атома, восстанавливается, а другой атом хлора окисляется. [8]
Гидролиз хлора был впервые изучен А. А. Яковкиным ( 1863 - 1936), определившим константу равновесия этой реакции и степень гидролиза хлора при различных температурах. [9]
Для гидролиза хлора в хлорбензоле в присутствии 10 - 15 % - ного раствора едкого натра необходима температура порядка 350 С. [10]
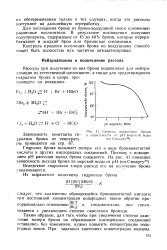 |
Степень выделения брома. [11] |
Вследствие гидролиза хлора расход его на получение брома увеличивается. [12]
Равновесие гидролиза хлора сдвигается в правую сторону, новые порции хлора растворяются с образованием хлорноватистой кислоты. [13]
Равновесие гидролиза хлора сдвигается в правую сторону, новые порции хлора растворяются с образованием хлорноватистой кислоты. Таким образом, процесс электролиза направлен не в сторону образования хлора и каустической соды, а протекает с образованием гипохлорита натрия. [14]
Вследствие гидролиза хлора в нем находятся соляная и хлорноватистая кислоты. В тех случаях, когда электролит подщелачивают, растворенный хлор и хлорноватистая кислота образуют гипо-хлорит натрия. Некоторое количество соляной кислоты образуется в электролите в результате разряда кислорода на аноде и при электролитическом и химическом образовании хлоратов. Происходящий на катоде побочный процесс выделения водорода приводит к снижению кислотности электролита. [15]
Страницы: 1 2 3 4