Гидролиз - хлор
Cтраница 2
Вследствие гидролиза хлора в рассоле находятся соляная и хлорноватистая кислоты. При подщелачивании электролита растворенный хлор и хлорноватистая кислота образуют ги-похлорит натрия. Некоторое количество соляной кислоты образуется в электролите в результате разряда кислорода на аноде и при электролитическом и химическом образовании хлоратов. Происходящий на катоде побочный процесс выделения водорода приводит к снижению кислотности электролита. [16]
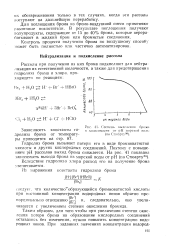 |
Степень выделения брома. [17] |
Вследствие гидролиза хлора расход его на получение брома увеличивается. [18]
Процесс гидролиза хлора водой протекает в течение примерно 2 минут. Если хлор пропускать в воду, в которой находится мел во взвешенном состоянии, то в результате реакции все время будет увеличиваться концентрация хлорноватистой кислоты в растворе, а равновесие реакции сместится слева направо. [19]
Процесс гидролиза хлора по этому уравнению может идти непрерывно лишь тогда, когда вся хлорноватистая кислота связывается олефином в хлоргидрин. Концентрация же хлористого водорода, образующегося при гидролизе хлора, не уменьшается, а наоборот, растет по мере того, как реакция прогрессирует. [20]
Процесс гидролиза хлора по этому уравнению может идти непрерывно лишь тогда, когда вся хлорноватистая кислота связывается олефином в хлоргидрин. Концентрация же хлористого водорода, образующегося при гидролизе хлора, но уменьшается, а наоборот, растет по мере того, как реакция прогрессирует. [21]
Процесс гидролиза хлора подробно изучен А. В концентрированном соляном растворе, который применяется для электролиза, концентрация хлорноватистой кислоты, как видно из уравнения ( 1), будет еще меньше. [22]
Степень гидролиза хлора в водном растворе увеличивается с повышением температуры и уменьшается с повышением концентрации. В присутствии хлоридов и кислот степень гидролиза хлора существенно уменьшается. При повышении величины рН до 3 и выше хлорная вода практически не содержит молекулярного хлора. [23]
Процесс гидролиза хлора водой протекает в течение примерно 2 минут. Если хлор пропускать в воду, в которой находится мел во взвешенном состоянии, то в результате реакции все время будет увеличиваться концентрация хлорноватистой кислоты в растворе, а равновесие реакции сместится слева направо. [24]
О гидролизе хлора / / Журн. [25]
Эти продукты гидролиза хлора весьма агрессивны по отношению к металлическим и неметаллическим материалам, степень агрессивности определяется в основном концентрацией в нем влаги. [26]
На процесс гидролиза хлора влияние оказывают: температура хлорной воды, рН раствора, наличие света и катализаторов, интенсивность перемешивания жидкой и газообразной фаз при абсорбции хлора водой. С повышением температуры воды равновесие реакции гидролиза сдвигается вправо. Максимальный сдвиг происходит при 90 С. [27]
О механизме гидролиза хлора, Журн. [28]
Получающиеся при гидролизе хлора НС1 и НОС1 могут взаимодействовать друг с другом, снова образуя хлор и воду, поэтому реакция не идет до конца; равновесие устанавливается, когда прореагирует приблизительно / з растворенного хлора. Таким образом, хлорная вода всегда содержит наряду с молекулами С12 значительное количество соляной и хлорноватистой кислот. [29]
Получающиеся при гидролизе хлора НС1 и НС10 могут взаимодействовать друг с другом, снова образуя хлор и воду, поэтому реакция не идет до конца; равновесие устанавливается, когда прореагирует приблизительно Уз растворенного хлора. Таким образом, хлорная вода всегда содержит наряду с молекулами С12 значительное количество соляной и хлорноватистой кислот. [30]
Страницы: 1 2 3 4