Гидролиз - метиловый эфир
Cтраница 3
В 2 3 5-триметиларабинозе содержится фурановый цикл. Положение кислородного мостика в элементарных звеньях макромолекул арабана, которые при гидролизе метилового эфира арабана дают 2 3-диметиларабинозу, остается не выясненным. Принимая во внимание легкую гидролизуемость арабана, Херст считает, что в макромолекуле арабана содержатся только арабо-фурановые циклы. [31]
Так как 8к2 - реакции проходят медленно, то алкил-кислородный разрыв не наблюдается, например при гидролизе метиловых эфиров. [32]
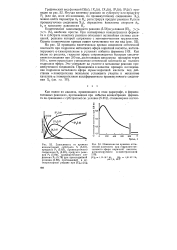
Как видно из рисунка, гидролиз эфира сопровождается быстрым увеличением поглощения при 310 нм, достигающим максимума примерно через 100 с, затем происходит уменьшение оптической плотности до полного гидролиза эфира. Это указывает на участие в механизме реакции промежуточного соединения. Приведенное в качестве примера исследование гидролиза метилового эфира транс-коричной кислоты под действием а-химотрипсина позволило установить участие в механизме катализа а-химотрипсином ацилферментного промежуточного соединения Х2 ( см. гл. [34]
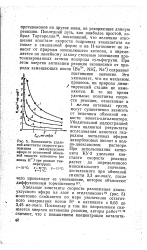 |
Зависимость удельной константы скорости раз - Жжения диазоуксусного эфира от остаточной обменной емкости катеонита ( по ионам Н при разных температурах. [35] |
Это указывает, что ни механизм, процесса, ни природа лими - / тирующей стадии не изменяются. В то же время удельные константы скорости реакции, отнесенные к 1 мг-экв активных групп, могут существенно зависеть от величины обменной емкости ионита-катализатора. Убедительной иллюстрацией этого являются результаты исследования кинетики гидролиза метиловых эфиров дикарбоновых кислот в вод-но-диоксановом растворе. [36]
В подтверждение правильности структур, приписанных метил-ликоктонамату CDLXXVIII иметилоксиликоктонаматуСВЬХХ1Х, было найдено, что CDLXXVIII гидролизуется гораздо легче, чем CDLXXIX. Причина этого различия становится ясной лишь при изучении молекулярных моделей, которые показывают, что водород и метоксигруппа при G-6 вызывают большие пространственные затруднения по G-17 в случае CDLXXIX, чем в случае CDLXXVIII. Конфигурация карбоксильной группы при С-4 в метиловом эфире винатикойевой кислоты CDLXXX была установлена [245] путем определения скорости его омыления и сравнения со скоростью гидролиза метилового эфира подокарповой кислоты, в котором карбоксильная группа сильно затруднена, так как находится в г с-ориентации по отношению к ангулярной метильной группе. [37]
Реакции 2 4 6-триметилбензойной кислоты и ее эфиров в серной кислоте характеризуются быстрым и полным образованием ацилий-иона. Действительно, в тех случаях, когда удается исследовать кинетику реакций, оказывается, что ацилий-ион должен образовываться медленно, поскольку он определяет скорость всего процесса, а стационарная концентрация его может быть очень мала. Кинетика гидролиза метилового эфира и-толуиловой кислоты весьма сходна с приведенной выше, но скорость реакции в этом случае в 4 раза больше. Подобная картина, как упоминалось выше, имеет место для тг-нитрофенилацетата в среде, содержащей до 30 % воды. Бендер [51] установил, что метиловый эфир 2 4 6-триметилбензойной кислоты гидролизуется в 3 Ж водном растворе серной кислоты по механизму Аде. [38]
Но можно решить почти эквивалентную обратную задачу: пометить все те кислородные атомы моносахаридного остатка, которые не использованы для образования гликозидных связей и циклов. Это достигается методом метилирования. Идея метода заключается в том, что метиловые эфиры Сахаров устойчивы в условиях кислотного гидролиза гликозидных связей. Поэтому после гидролиза метилового эфира полисахарида можно получить метиловые эфиры входящих в его состав моносахаридов, причем метиль-ные группы в них окажутся в тех же самых положениях, в которых они были в соответствующих моносах аридных остатках полисахаридной цепи. Напротив, неметилированными в них будут те гидроксилы, которые были использованы для образования гликозидных связей и освободились при гидролизе. Таким образом, установив строение метилированных моносахаридов и, следовательно, положение в них метильных групп, можно выяснить, какими своими положениями эти моносахариды были связаны в исходной полисахаридной цепи. [39]
Страницы: 1 2 3