Гидроокись - литий
Cтраница 2
Гидроокись лития применяется как электролит для аккумуля - TODOB с большой электрической емкостью, а также для приготовления фотографических проявителей. [16]
Гидроокись лития, необходимая для получения литиевых мыл, в настоящее время не является дефицитным продуктом. Интересно отметить, что это связано с развитием ядерной техники. [17]
Гидроокиси лития и натрия, нанесенные на активированный уголь, несколько тормозят реакции крекинга и усиливают реакции дегидрирования, a гидроокись калия вызывает значительное торможение обеих реакций. [18]
Гидроокись лития и ее концентрированные растворы уже при обычной температуре разрушают стекло и фарфор [26], что делает необходимым парафинирование тары. В расплавленном состоянии LiOH можно получить только в никелевых или серебряных сосудах, так как она окисляет [10, 29] многие металлы ( железо, платину и др.), сплавы ( монель-металл разрушается даже в восстановительной атмосфере) и другие материалы. [19]
Гидроокись лития гораздо менее гигроскопична, чем едкий натр и едкое кали. Из водного раствора она кристаллизуется в виде гидрата LiOH Н2О, который может быть тонко измельчен. Растворимость гидроокиси лития в воде примерно в 5 раз ( по весу) меньше растворимости едкого натра и едкого кали. С другой стороны, гидроокись лития примерно в 100 раз более растворима, чем гидроокись кальция, и почти в 4 раза более растворима, чем гидроокись бария. Подобно едкому натру и едкому кали, гидроокись лития может быть расплавлена. Склонность к разложению при нагревании выражена у нее не так резко, как в случае гидроокисей щелочноземельных металлов. Температура плавления гидроокиси лития, равная 445, намного превышает температуры плавления гидроокисей остальных щелочных металлов. [20]
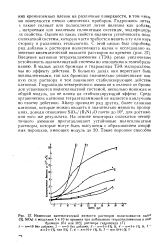 |
Изменение кинематической вязкости растворов полисиликатов кали ( % SiCb с модулями 5 и 10 во времени при добавлении тетраэтиламмония в виДе. [21] |
Гидроокись лития 1 также силикат или полисиликат лития полезны как добав, натриевым или калиевым силикатным системам, модифицируя свойства. Одним из таких свойств является устойчивость поли-силикатной системы, которую часто требуется менять в ту или иную сторону в различных технологиях. Введение катионов тетраэтиламмония ( ТЭА) резко увеличивает устойчивость полисиликатной системы по отношению к гелеобразо-ванию. В малых дозах бромиды и гидроксиды ТЭА малоразличимы по эффекту действия. В больших дозах они перестают быть эквивалентными, так как бромиды значительно увеличивают ионную силу раствора и тем понижают стабилизирующее действие катионов. Гидроксиды четвертичного аммония в отличие от бромидов усваиваются полисиликатной системой, несколько понижая ее общий модуль, но не влияя на стабилизирующий эффект. Среди органических катионов тетраэтиламмоний не является наилучшим по своему действию. Дилер приводит ряд других, более сложных катионов, которые можно вводить в значительно меньших пропорциях, доводя отношение SiCb / ( R4N) 2О почти до 103, для достижения того же результата. [22]
Гидроокись лития LiOH образуется при растворении металлического лития, его окиси, сульфида, нитрида и фосфидов лития в воде. [23]
Гидроокись лития LiOH образуется при действии металла на воду или при взаимодействии сульфата лития с гидратом окиси бария. Бесцветные кристаллы LiOH Н2О теряют кристаллизационную воду при нагревании в токе водорода. [24]
Гидроокись лития LiOH - бесцветные кристаллы тетрагональной сингонии; а 3 549 А, с - 4 334 А; плотн. В воде LiOH растворима менее гидроокисей др. щелочных элементов. [25]
 |
Железо-никелевый аккумулятор с болтовым креплением пластин. [26] |
Действие гидроокиси лития не вполне выяснено. Электропровод, ность раствора в присутствии его уменьшается примерно на 20 %; казалось бы, что добавка гидроокиси лития должна сказываться отрицательно. При работе аккумулятора содержание гидроокиси лития в растворе уменьшается. [27]
Получение гидроокиси лития каустификацией Li2CO3 связано с расходом только доступных и дешевых материалов. [28]
Кристаллы гидроокиси лития ( LiOH) имеют ту же симметрию и такое же число атомов в элементарной ячейке и, следовательно, те же правила отбора в спектрах. [29]
Раствор гидроокиси лития введен через рот в дозе 0 5 мг / г. Погибла на 2 - е сутки. [30]
Страницы: 1 2 3 4