Кристаллическая гидроокись
Cтраница 3
При получении активной окиси алюминия конечный продукт ( f - Alz03 образуется в результате разложения кристаллической гидроокиси алюминия. Пористой структурой гидроокиси определяется формирование только крупных пор в готовом контакте. Тонкая пористая структура предопределяется условиями дегидратации гидроокиси и не зависит от ее пористой структуры. [31]
При получении активной окиси алюминия конечный продукт ( f - - Aijp3 образуется в результате разложения кристаллической гидроокиси алюминия. Пористой структурой гидроокиси определяется формирование только крупных лор в готсзом контакте. Тонкая пористая структура предопределяется условиями дегидратации гидроокиси и не зависит от ее пористой структуры. [32]
Проверим, можно ли различные реакционные способности взаимодействия щелочных металлов с водой объяснить различиями в энтальпиях растворения их кристаллических гидроокисей. [33]
По кривым разложения установлены аналогии между диаспорой, бемитом и гид-раргиллитом ( гиббситом), с одной стороны, и кристаллическими гидроокисями железа - гетитом, лепидкроки-том и рубиновой слюдой - с другой. Кристаллы гидроокисей превращаются в поликристаллические агрегаты окисей в продуктах - серий; однако отдельные индивидуумы ориентированы. [34]
Лучше использовать воду - это дает возможность избежать применения агрессивных сред ( кислот, щелочей), а также сразу получить кристаллическую гидроокись алюминия, легко отделяемую от спиртов. Однако при этом возможно образование побочных продуктов. [35]
Эта операция состоит в выделении осадка А1 ( ОН) 3 из раствора алюмината после его разбавления и введения в него затравки кристаллической гидроокиси A. Эта процедура приводит к образованию хорошо фильтрующего мелкокристаллического осадка. [36]
Для первого из них можно было бы написать в ионной фо рме ( NI-I) ( ОН) подобно тому, как пишется Ка ( ОН -) для кристаллической гидроокиси натрия. [37]
В колбу Вюрца на 500 мл, соединенную с холодильником и снабженную термометром, шарик которого на 5 мм не доходит до дна колбы, помещают хорошо перемешанную смесь 100 г адипиновой кислоты и 5 г кристаллической гидроокиси бария. [38]
В колбу Вюрца вместимостью 500 мл, соединенную с холодильником и снабженную термометром, шарик которого на 5 мм не доходит до дна колбы, помещают хорошо перемешанную смесь 100 г адипино-вой кислоты и 5 г кристаллической гидроокиси бария. [39]
В колбу Вюрца на 500 мл, соединенную с холодильником и снабженную термометром, шарик которого на 5 мм не доходит до дна колбы, помещают хорошо перемешанную смесь 100 s адипиновой кислоты и 5 г кристаллической гидроокиси бария. [40]
Для приготовления 0 05; 0 1 и 0 2 моль / дм3 растворов гидроокиси калия ( 3 0 0 1), ( 6 0 0 1) и ( 12 0 0 2) г кристаллической гидроокиси калия помещают в круглодонную колбу вместимостью 2000 см3 с обратным холодильником, растворяют в 1000 см3 изопропанола или этилового спирта и нагревают до кипения в течение 10 мин. Раствор защищают от доступа углекислого газа, снабжая бутылку трубкой с раствором натронной извести или другим веществом, поглощающим углекислый газ. Раствор не должен соприкасаться с резиновой пробкой, закрывающей бутылку или со смазкой, уплотняющей стеклянную пробку. [41]
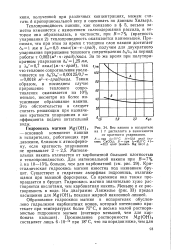 |
Вес накипи в испарителе. [42] |
Магнезиальная накипь отличается от карбонатной большей плотностью и теплопроводностью. Кристаллическая гидроокись магния известна под названием бруцит. Существует и гидратная аморфная гидроокись, отлагающаяся при высокой форсировке. Со временем она также превращается в бруцит. Гидроокись магния значительно хуже растворяется кислотами, чем карбонатная накипь. [43]
Порошок кристаллической гидроокиси алюминия обычно смачивается любыми низкомолекулярными органическими кислотами. [44]
Кроме того, оно может быть связано с большей рассосредото-ченностью новообразований, потому что частично последние могут кристаллизоваться на поверхности глины и, следовательно, меньше задерживать гидратацию в начальные сроки; в то же время быстрее растворяться и перекристаллизовываться в случае термодинамической неустойчивости. Более раннее появление кристаллической гидроокиси кальция при невысоких температурах гидратации, когда ее поглощение глиной не успевает следовать за накоплением ионов кальция и ОН -, возникающих в результате гидратации, также свидетельствует об ускоренном, по сравнению с чистым G S или цементом, разложении вяжущего в присутствии палыгорскита. Это хорошо согласуется с данными работы [369], так как при гидратации QS с аэросилом происходят аналогичные явления. После затворения понижена концентрация ионов кальция и уменьшено рН, зато увеличивается концентрация силикатных ионов. Однако через 60 мин ( при нормальной температуре) концентрация Са2 в системе повышается примерно в два раза по сравнению с такой же суспензией QS без аэросила. При этом в пастах с аэросилом образуются несколько раньше и отличные по форме от обычных гидратов новообразования с извилисто-фольговым типом частиц. [45]
Страницы: 1 2 3 4