Гидроперекись - ацетило
Cтраница 3
К 130.5 углеводорода в 340 мл абсолютного эфира постепенно при температуре не выше 25 прибавлено 65 г 93 %, а затем 113 г 80 % гидроперекиси ацетила из расчета 2 атома кислорода на 1 молекулу углеводорода. [31]
Поэтому более вероятное предположение относительно образования эфира циклопентенолфосфиновой кислоты - это отщепление уксусной кислоты при перегонке от продукта присоединения уксусной даислоты к окиси в процессе окисления гидроперекисью ацетила. [32]
Многочисленные способы, предложенные для получения холо-целлюлозы, могут быть сведены к трем методам, основанным на окислении хлором, двуокисью хлора или хлоритом натрия и гидроперекисью ацетила или ацетона. [33]
Хлористый бензоил можно превратить в перекись бензоила, а перекись бензоила - в его гидроперекись, называемую надбен-зойной кислотой, так же, как из хлористого ацетила получают перекись и гидроперекись ацетила ( см. стр. Надбензойную кислоту применяют в лабораторной практике в качестве окислителя. [34]
Эти недостатки искупаются, однако, надежностью получаемых результатов, так как все углеводороды предельного характера ( парафины, нафтены, ароматика) совершенно не реагируют с гидроперекисью бензоила и гидроперекисью ацетила. [35]
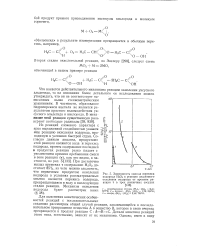 |
Зависимость выхода перекиси водорода Н2О2 в реакции медленного окисления водорода от времени реакции t в трех различных сосудах. [36] |
Что касается действительного механизма реакции окисления уксусного альдегида, то на основании более детального ее исследования можно утверждать, что он не соответствует написанным выше стехиометрическим уравнениям. В частности, образование гидроперекиси ацетила не является результатом простого взаимодействия уксусного альдегида и кислорода. [37]
Некоторые производные окиси этилена, получающиеся по этому способу, оказываются стойкими при гидролизе. В таких, случаях Ббзекен и Элсен5 рекомендуют пользоваться гидроперекисью ацетила, так как при этом в качестве продуктов окисления сразу получаются ацетаты гликолей. [38]
Гидроперекись бензоила, СвН5 - СО - О2Н, при нагревании разлагается, как указано Эрленмейером, со взрывом на кислород и бензойную кислоту. Гидроперекись пропионила, СН3СН8СО3Н, значительно более стабильна 16 чем гидроперекись ацетила. [39]
Некоторые производные окиси этилена, получающиеся по этому способу, оказываются стойкими при гидролизе. В таких, случаях Бдзекен и Э л с е н 5в рекомендуют пользоваться гидроперекисью ацетила, так как при этом в качестве продуктов окисления сразу получаются ацетаты гликолей. [40]
Наиболее часто применяемые методы делигнификации растительной ткани основаны на окислении лигнина различными окислителями с образованием растворимых в воде продуктов. В качестве окислителей могут служить водные растворы: хлора, двуокиси хлора, хлорита натрия, гидроперекиси ацетила ( надуксусная кислота), гидроперекиси ацетона и др. Остаток ткани после делигнификации принято называть холоцеллюлозой. Холоцеллюлоза должна содержать всю целлюлозную и гемицеллюлозную часть растительной ткани по возможности в химически неизменном состоянии. Практически такой продукт получить почти невозможно. Обычно при всех применяемых методах делигяификации теряется часть полисахаридов и остается в холоцеллюлозе некоторое количество лигнина. Возможны также изменения в составе гемицеллюлоз, частичное окисление углеводов, некоторая деструкция целлюлозы. Все эти факторы необходимо учитывать при установлении химического состава полисахаридов гемицеллюлоз. [41]
Было установлено, что небольшие количества днэтилпере-киси ( CaHsOOCjjHs) или этилгидроперекиси ( СаНзООН) вызывают очень сильную детонацию, которая практически полностью подавляется добавлением тетраэтилсвннца. Ацеталь - дегид сам по себе не оказывал влияния на детонацию, но при добавлении его вместе с гидроперекисью ацетила ( СНзСОООН) наступала резко выраженная детонация: такое же действие оказывала одна гидроперекись ацетила. [42]
Было установлено, что небольшие количества днэтилпере-киси ( CaHsOOCjjHs) или этилгидроперекиси ( СаНзООН) вызывают очень сильную детонацию, которая практически полностью подавляется добавлением тетраэтилсвннца. Ацеталь - дегид сам по себе не оказывал влияния на детонацию, но при добавлении его вместе с гидроперекисью ацетила ( СНзСОООН) наступала резко выраженная детонация: такое же действие оказывала одна гидроперекись ацетила. [43]
Такого рода остановка реакции окисления при неизрасходованном значительном количестве исходных продуктов, как показал Н. М. Эмануэль [33], весьма характерна для многих случаев окисления. К этому выводу Н. М. Эмануэль пришел, анализируя опытные данные других авторов по окислению углеводородов и альдегидов и свои собственные опыты по окислению уксусного альдегида при 200 и давлении 100 мм рт. ст. В избытке кислорода окисление альдегида, приводящее к гидроперекиси ацетила, как основному продукту реакции, прекращается, когда израсходовано около половины альдегида, и в системе остается достаточно кислорода. После этого кислород перестает расходоваться и идет лишь реакция окисления альдегида полученной перекисью. Эта новая цепная реакция также прекращается ранее, чем весь альдегид окажется израсходованным. Далее реакция не идет, несмотря на наличие кислорода и альдегида в системе. Химический механизм подобных явлений подробно не исследован. Продукт, тормозящий реакцию, еще неизвестен, однако общие обоснования в виде теории вырожденных разветвлений позволяют понять их природу. [44]
С применением окислительно-восстановительных систем более широко стали использоваться в качестве инициаторов гидроперекиси. Некоторые гидроперекиси распадаются с образованием свободных радикалов достаточно быстро и не требуют активаторов; для эффективного применения других гидроперекисных инициаторов необходимо присутствие восстановителя. Гидроперекись ацетила ( надуксусная кислота) растворима в воде, и поэтому для получения наилучших результатов ее следует применять для инициирования полимеризации мономеров, растворимых в воде. [45]
Страницы: 1 2 3 4