Гидроперекись - метил
Cтраница 1
Гидроперекиси метила и этила-малоустойчивые соединения, сильно взрывают. Более устойчивы гидроперекиси, содержащие вторичные радикалы, например гидроперекись изопропила ( СН3) 2СН - О-О - Н и гидроперекись mpem - бутила ( СН3) 3С - О-ОН. [1]
Гидроперекись метила СН3 - О-О - Н перегоняется при осторожном нагревании в вакууме ( 65 мм рт. ст.) при 38 - 40 С. [2]
Гидроперекиси метила и этила - малоустойчивые соединения, сильно взрывают. Более устойчивы гидроперекиси, содержащие вторичные радикалы, например гидроперекись изопропила ( СН3ЬСН - О-О - Н и гидроперекись грет-бутила ( СИз) зС - О-ОН. [3]
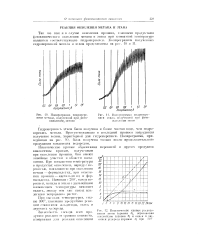
Образование гидроперекиси метила из метана, облученного рентгеновскими лучами ( 200 кв) в водном растворе в присутствии растворенного кислорода. [4]
Так, гидроперекись метила и диметилперекись крайне неустойчивы, в то время как перекись ди - mpem - бутила можно перегонять при атмосферном давлении. Перекись ацетила легко взрывается, а перекись бензоила стабильна. Например, гидроперекиси - бутила и изобутила при температурах от 90 до 100 разлагаются с выделением кислот и водорода, а гидроперекись mpem - бутила дает кислород и mpem - бутиловый спирт. В паровой фазе при температуре около 300 гидроперекись mpem - бутила дает mpem - бутиловый спирт, метиловый спирт, ацетон, формальдегид, метан и воду. [5]
Смесь диметилперекиси с гидроперекисью метила при 114 С светится вначале тем же красным светом, а после поглощения кислорода надолго зажигается в десятки раз более интенсивное формальдегидное свечение. [6]
Более устойчивая, чем гидроперекись метила, она тем не менее сильно взрывает при нагревании. Смешивается с водой и с органическими растворителями. [7]
Таким образом, при использовании гидроперекиси метила кислород не участвует в возбуждении формальдегидного свечения. [8]
Фок и Налбандян 7 ] выделили гидроперекись метила из продуктов фотохимического окисления при низких температурах. [9]
Продуктами окисления метана являются довольно значительные количества гидроперекиси метила ( до 0 3 % на пропущенный метал) и формальдегид. Те же продукты образуются и при фотохимическом ( освещение светом Шумановской области спектра) окислении метана. В этой области спектра метан прозрачен, а кислород диссоциирует на атомы. [10]
Взрывчатый характер, очень сильно проявляющийся в случае гидроперекисей метила и этила, ослабевает с увеличением молекулярного веса гидроперекисей. [11]
При этих условиях в продуктах окисления также не обнаруживается гидроперекись метила. [12]
 |
Подпрограмма гидропере. [13] |
Гидроперекись этила была получена в более чистом виде, чем гидроперекись метила. [14]
Было доказано даже в случае метана и этана, что продуктами реакции являются гидроперекиси метила СН3ООН и соответственно этила СгН6ООН, которые были выделены в чистом состоянии. Нормальное горение углеводородов также протекает с первоначальным образованием гидроперекисей. [15]
Страницы: 1 2 3