Гидрохлорид - гидроксиламин
Cтраница 3
Приготовляют 1 % - ный раствор гидрохлорида гидроксиламина и нейтрализуют его аммиаком по метиловому красному. Затем на каждые 100 мл СНС1з или СС14 прибавляют по 10 мл приготовленного нейтрализованного раствора гидрохлорида гидроксиламина; жидкость переносят в делительную воронку, взбалтывают и сливают нижний слой органического растворителя. Эту операцию повторяют еще 1 - 2 раза и очищенный таким образом реактив перегоняют, поместив перегонную колбу на водяную баню. [31]
Приготовляют 1 % - ный раствор гидрохлорида гидроксиламина и нейтрализуют его аммиаком по метиловому красному. Затем на каждые 100 мл СНС13 или СС14 прибавляют по 10 мл приготовленного нейтрализованного раствора гидрохлорида гидроксиламина; жидкость переносят в делительную воронку, взбалтывают и сливают нижний слой органического растворителя. Эту операцию повторяют еще 1 - 2 раза, и очищенный таким образом реактив перегоняют, поместив перегонную колбу на водяную баню. [32]
Приготовляют 1 % - ный раствор гидрохлорида гидроксиламина и нейтрализуют его аммиаком по метиловому красному. Затем на каждые 100 мл СНСЬ или ССЦ прибавляют по 10 мл - приготовленного нейтрализованного раствора гидрохлорида гидроксиламина; жидкость переносят в делительную воронку, взбалтывают и сливают нижний слой органического растворителя. Эту операцию повторяют еще 1 - 2 раза, и очищенный таким образом реактив перегоняют, поместив перегонную колбу на водяную баню. [33]
Суспензию 5 г 6-нитрохинолина и 6 г гидрохлорида гидроксиламина в 90 мл спирта обрабатывают 30 мл 20 % - ного раствора едкого кали в метаноле. Выделяется осадок хлорида калия, раствор окрашивается в желтый цвет и вскоре выделяется кристаллическое вещество. [34]
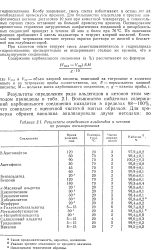 |
Результаты определения альдегидов и кетонов. [35] |
При холостом опыте титруют смесь диметиламиноэтанола и гидрохлорида гидроксиламина; предварительно ее выдерживают столько же времени, что и анализируемое соединение. [36]
Растворяют в воде 20 - 30 мг гидрохлорида гидроксиламина и смешивают с приготовленным таким же образом раствором хлорида никеля. Охлаждают в бане со льдом и приливают несколько капель диацетила. При добавлении охлажденного во льду раствора аммиака осаждается красное комплексное соединение никеля с диметилглиоксимом. [37]
Исходный раствор I: 2 5 г гидрохлорида гидроксиламина растворяют в 7 5 мл воды. Раствор разбавляют спиртом до 25 мл. Исходный раствор II: 5 г едкого кали растворяют в минимальном количестве воды. Раствор разбавляют спиртом до 50 мл. [38]
Две порции 10 % - ного раствора гидрохлорида гидроксиламина, по 10 мл каждая, вносятся пипеткой в две конические колбы вместимостью 125 мл. Если в пробе имеются смолистые вещества или осадки, то в качестве растворителя в стаканчик добавляют 10 мл метанола. Такой же объем последнего прибавляют и во вторую ( сравнительную) колбу. Конец титрования фиксируется по переходу желтой окраски в светло-пурпуриую. В некоторых случаях определение ведут в растворе пиридина. [39]
Суспензию 5 г 6-нитрохинолина и 6 г гидрохлорида гидроксиламина в 90 мл спирта обрабатывают 30 мл 20 % - ного раствора едкого кали в метаноле. Выделяется осадок хлорида калия, раствор окрашивается в желтый цвет и вскоре выделяется кристаллическое вещество. [40]
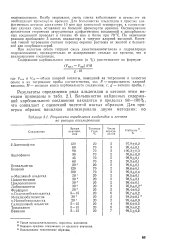 |
Результаты определения альдегидов и кетонов. [41] |
При холостом опыте титруют смесь диметиламиноэтанола и гидрохлорида гидроксиламина; предварительно ее выдерживают столько же времени, что и анализируемое соединение. [42]
Ионы Си2 восстанавливают до ионов Си добавлением гидрохлорида гидроксиламина. Ионы Си реагируют с неокупроином в нейтральной или слабокислой среде с образованием комплексного соединения, в котором на 1 моль Си приходится 2 моль неокупроина. Это соединение может быть извлечено различными органическими растворителями, в том числе хлороформом. [43]
В 2 мл воды растворяют 1 г гидрохлорида гидроксиламина и 1 г ацетата натрия. [44]
При титровании основанием смеси борной кислоты с гидрохлоридом гидроксиламина сначала протекает реакция с гидрохлоридом. В течение этой реакции электропроводность раствора мало изменяется, потому что мало различаются подвижности ионов, заменяющие друг друга в растворе. После второй точки эквивалентности электропроводность сильно увеличивается от избытка основания. [45]
Страницы: 1 2 3 4