Атомистическая гипотеза
Cтраница 3
Таким образом, развивая теорию Дэви и Авогадро, связав ее с атомистической гипотезой, Берцелиус в значительной степени содействовал обоснованию и утверждению атомистической гипотезы не только соображениями химического порядка, но также соображениями электрохимического порядка. [31]
Не случаен тот факт, что именно в 1812 - 1913 гг. Берцелиус, применяя впервые понятие об атомном весе, начинает пользоваться атомистической гипотезой. Именно к этому времени выкристаллизовалась его электрохимическая теория, которая, так же как химические пропорции и законы Гей-Люсса - ка, вела к корпускулярной теории строения вещества, восполнив пробел атомистики Дальтона в области теории химического сродства. [32]
Обычная версия на этот счет гласит, будто бы Дальтон сначала открыл закон кратных отношений, а затем, стремясь его теоретически объяснить, воспользовался атомистической гипотезой. [33]
Количественные исследования химического состава различных веществ во времена Ломоносова только еще начинались, и не было еще никакого эмпирического материала, необходимого для проверки и подтверждения атомистической гипотезы в химии. [34]
Во-первых, необходимо отметить, что сам Гей-Люссак опирался на объемные данные при выражении состава сложных веществ, в частности, органических; но он избегал связывать эти отношения с атомистической гипотезой. Анализ органических веществ легко приводил к применению объемных методов исследований, ибо расчеты химического анализа были связаны с определением объемов углекислого газа и воды. [35]
Обычная версия на этот счет гласит, будто Дальтон сначала чисто эмпирическим путем открыл на основании химических анализов закон кратных отношений, а затем, стремясь его объяснить, воспользовался атомистической гипотезой. [36]
В 1810 г. во второй части своей работы Новая система химической философии Дальтон решительно выступил против открытого Гей-Люссаком закона объемных отношений, увидев в нем не подтверждение, а угрозу своей атомистической гипотезе. [37]
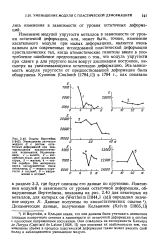
Изменение модулей упругости металлов в зависимости от уровня остаточной деформации, или, может быть, точнее, изменение касательного модуля при малых деформациях, является очень важным для современных исследований пластической деформации кристаллических тел, когда атомистические гипотезы ввели в употребление ошибочное предположение о том, что модуль упругости при сдвиге ц, для упругого поля вокруг дислокации постоянен, несмотря на увеличивающуюся остаточную деформацию. [39]
Обобщая взгляды Берцелиуса в 1818 - 1820 гг. на основные положения атомистической гипотезы, необходимо подчеркнуть, что благодаря Берцелиусу, синтетически объединившему в одно целое все выводы, вытекавшие из химических пропорций, объемных законов и электрохимических данных, атомистическая гипотеза получила прочную эмпирическую опору, что позволило ей завоевать доверие и признание химиков мира. Вместе с тем понятие об атомном весе стало более резко отличаться от понятия об эквивалентах и пропорциональных числах. Тем более, что формулы кислот и оснований Берцелиуса ( 1819) не были эквивалентны между собой. [40]
Атомистическая гипотеза о строении вещества была высказана еще в античное время. Научное же обоснование она получила сравнительно недавно, когда был открыт фундаментальный закон химии - закон кратных отношений. [41]
Атомистическая гипотеза в Англии, сравнительно с. Этому немало способствовали труды выдающихся английских атомистов - Бойля, Ньютона и других. Атомистическая теория была чрезвычайно близка и Хиггинсу, который применил ее для объяснения некоторых химических явлений. [42]
Законы химического соединения легко понять, если допустить, что: ( 1) каждый элемент состоит из мельчайших неделимых частиц, атомов, причем все атомы данного элемента совершенно одинаковы и, что особенно важно, имеют одинаковый вес; ( 2) образуя соединение, некоторое число ( обычно малое) атомов разного рода соединяется определенным образом в молекулы; ( 3) соединение представляет собой агрегат таких молекул, состав которых для данного соединения совершенно одинаков. Атомистическая гипотеза строения материи, однако, опередила открытие законов, по которым элементы соединяются, и уже некоторые ученые древности считали, что материя состоит из атомов. Тем не менее едва ли можно считать, что они сформулировали настоящую научную теорию; следует считать началом современной атомистической теории вывод Дальтоном законов химического соединения и данное им описание химических соединений и реакций на основе атомных представлений. [43]
Ломоносов с увлечением занимается этой работой в Физическом кабинете Академии наук, дома и с 1748 г. в созданной им Химической лаборатории. Его атомистическая гипотеза углубляется и уточняется, теперь он уже называет ее системой корпускулярной философии. [44]
Необходимо отметить, что А. М. Бутлеров в своем докладе подчеркивает выражения химические атомы и химическое строение и даже противопоставляет, как это он делал и впоследствии, химические атомы физическим. Бутлерова атомистическая гипотеза была вероятной, и он выражал уверенность, что в будущем будет возможным определять пространственное расположение атомов в частице. Однако считая, что это при современном ему состоянии науки еще невыполнимо, А. М. Бутлеров предпочел говорить о химических атомах, или наименьших количествах элементов, входящих в состав частиц, и химическом строении, или о познаваемом из опыта порядке их связи в частице, а не о конституции в смысле Жирара и Кольбе. [45]
Страницы: 1 2 3 4