Глесстон
Cтраница 1
Глесстон 16в 217, Хиклинг и Солт 1во 195 218 и Шульди-нер 206 212 219 измеряли потенциал электрода непосредственно после выключения поляризующего тока. [1]
Глесстон ( 1924) и Хик-линг ( 1941), то оба метода дают результаты, совпадающие между собой в пределах ошибок опыта. Таким образом было доказано, что оба метода - и прямой, и коммутаторный - могут применяться для снятия поляризационных кривых. Совпадение результатов, полученных этими методами, указывает также на отсутствие особого переходного сопротивления и на кинетический характер явлений поляризации. [2]
Глесстон, Электрохимия растворов, гл. [3]
Глесстон, Введение в электрохимию, ИЛ, 1951, гл. [4]
Глесстон, Эйринг и Лейдлер предлагают гипотезу прототропи-ческого механизма перенапряжения. Это означает, что решающее значение приписывается процессу перескока протонов Н от одних молекул воды к другим молекулам воды. [5]
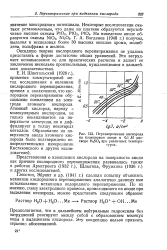 |
Перенапряжение кислорода на платиновом аноде в 0 1 М рас. [6] |
Глесстон, Эйринг и др. ( 1941 г.) сделали попытку объяснить механизм кислородного перенапряжения аналогично данному ими истолкованию механизма водородного перенапряжения. [7]
 |
Потенциалы выделения никеля при введении. нейтральных катионов. [8] |
Глесстон предложил теорию поляризации для частного случая выделения никеля. Согласно этой теории, поляризация обусловлена тем, что первичным продуктом разряда иона № 2 являются неустойчивые атомы с электронными уровнями 2, 8, 16, 2, обладающие собственным потенциалом, которые затем, с некоторой конечной скоростью, превращаются в стабильные атомы с уровнями 2, 8, 17, 1, обладающие другим потенциалом. [9]
Глесстон, Введение в электрохимию, Издатинлит, 1951, стр. [10]
Глесстон и Хиклинг [42, 43] связывали критический потенциал с поведением перекиси водорода на аноде и со скоростями ее взаимодействия с ацетат-ионом. [11]
Глесстон, Введение в электрохимию, ИЛ, 1951, гл. [12]
Глесстон С Лейдлер К. [13]
Глесстон и Хиклинг предполагают, что активным окислителем может быть также перекись водорода, как это упомянуто выше ( см. стр. [14]
Глесстон С, Введение в электрохимию. [15]
Страницы: 1 2 3 4