Глицидол
Cтраница 3
Аналогичным образом получают соответствующие глицидолы из фенилвинилкарбинола и додецил-пропенилкарбинола. [31]
Разнообразная реакционная способность глицидола 1 делает его популярным реагентом в органическом синтезе. [32]
Применение продуктов взаимодействия глицидола с соединениями, содержащими гидроксильные, карбоксильные, сульфамидные группы, амино - или карбоксиламидогруппы. [33]
В схеме выделения глицидола основной химической реакцией, определяющей потери продукта, является его полимеризация с образованием полиглицидола - водорастворимого полимера. Эта реакция может протекать как чисто термически, так и каталитически под влиянием кислот, оснований и солей. Технология выделения, концентрирования и осушки товарного глицидола должна разрабатываться в основном с учетом необходимости сведения к минимуму глубины протекания именно, этой реакции. [34]
Технологическая схема получения глицидола приведена на-рис. [35]
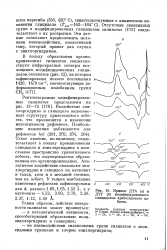 |
Кривые ДТА ( а и ДТГ ( б модифицированного глицидолом хризотилового асбеста. [36] |
Воздействие эшг-хлоргидрина и глицидола видоизменяет структуру хризотилового асбеста, что проявляется в изменении интенсивности рефлексов. Такое явление, по-видимому, свидетельствует в пользу проникновения глицидола и эпихлоргидрина в межслоевое пространство хризотилового з-асбеста, что подтверждается образованием его органопроизводных. Аналогичное воздействие оказывают эпи-хлоргидрин и глицидол на мусковит и тальк, хотя и в меньшей степени, чем на асбест. У талька наибольшие изменения рефлексов зафиксированы для d, равного 1.69 1.65 1.52 А, а у мусковита - 4.52, 3.89, 2.78, 2.56, 2.37, 1.72, 1.49 А. [37]
С эпихлоргидрином, глицидолом, окисью этилена и окисью пропилена обычные линейные продукты зтерификации образуют не только аминокислоты, но и белковые соединения, реагирующие таким же образом уже при комнатной температуре за счет свободных; арбоксильных групп. [38]
С эпихлоргидрином, глицидолом, окисью этилена и окисью пропилена обычные линейные продукты этерификации образуют не только аминокислоты, но и белковые соединения, реагирующие таким же образом уже при комнатной температуре за счет свободных карбоксильных групп. [39]
При действии азотной кислоты глицидол образует первичные или вторичные эфиры азотной кислоты или смесь этих эфиров. [40]
Таким образом, сам глицидол или его простейшие производные являются удобными объектами для получения большого набора нерацемических биологически активных соединений как традиционными, так и новейшими ( для данного круга соединений) методами. [41]
Когда в реакции используется скалемический глицидол, конфигурация хираль-ного центра С ( 2) исходной молекулы сохраняется у атома С ( 4) диоксоланового фрагмента, а энантиомерная чистота конечного продукта соответствует энантио-мерной чистоте исходного глицидола. Получающиеся по этой новой реакции кислородсодержащие гетероциклы могут найти применение в синтезе биологически активных соединений. [42]
Для получения фенилового эфира глицидола можно также прибавлять едкий натр к смеси фенола к эпихлоргидрина. Например, Фербурн, Гибссн и Стефенс304 прибавляли 297 г 27 % раствора едкого натра при 80 - - 100 к 188 г фенола и 185 г эпихлоргидрина. [43]
Глицериды получают также из глицидола или предварительным эпоксидированием сложных аллиловых эфиров с помощью перкислот и последующей этерификацией полученного эфира глицидола другими кислотами. [44]
Перспективными являются способы получения глицидола, основанные на окислении аллилового спирта гидропероксида-ми, пероксикислотами или пероксидом водорода. Низкая себестоимость последнего и преимущества, которые он дает в технологии получения глицидола, привели. [45]
Страницы: 1 2 3 4