Дизамещенные амид
Cтраница 3
Трибутиламин и диэтиланилин позволяют проводить эту реакцию при кипячении смеси реагентов в колбе. По данным Спейера [168], высокой каталитической активностью ( образование р-изомера) обладают М М - дизамещенные амиды кислот: М К-диметилформамид, N. Катализаторами этой реакции являются также и диалкшщианамиды [132] и высшие фенолы. [31]
Как видно из схемы, для внутримолекулярной циклизации необходимо наличие у амидного азота хоть одного водородного-атома. Поэтому монозамещепньте амиды ( IV, б) дают глубокое-изменение цвета, а дизамещенные амиды ( Г, в) свой цвет в присутствии щелочи не изменяют. Поскольку мои о - и дизамещенные амиды легко и быстро получаются из хлорангидрида дибензои-леппиридилнафтойпой кислоты ( III) и соответственно первичных или вторичных аминов, то эту реакцию можно использовать как качественную реакцию на первичные амины. [32]
Условно растворители разделяют на а п о л я р н ы е а п р о т о н - ные, биполярные апротонные и п р ото н н ы е растворители. К первой группе относят углеводороды, галогенпроизводные, третичные амины, сероуглерод; их диэлектрическая постоянная е меньше 15 и дипольный момент ц меньше 2 D. Биполярные апротонные растворители - N, Л / - дизамещенные амиды кислот, диме-тилсульфоксид, сульфоны, кетоны, нитрилы, нитропроизводные имеют е 15 и ц, 2 5 D. Протонные растворители - вода, спирты, амины, карбоновые кислоты, незамещенные амиды - являются донорами протонов при образовании водородных связей. [33]
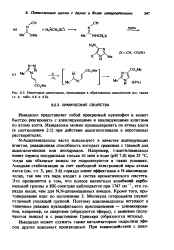 |
S. Некоторые циклизации, приводящие к образованию имидазолов ( также гл. 4, и. [34] |
Ацилимидазолы часто используют в качестве ацилирующих агентов, реакционная способность которых сравнима с таковой для ацилгалогенидов или ангидридов. Например, 1-ацетилимидазол имеет период полураспада только 41 мин в воде ( рН 7 0) при 25 С, тогда как обычные амиды не гидролизуются в таких условиях. N-ацилимида-золах, так как эта пара входит в состав ароматического секстета. Это проявляется в том, что полоса валентных колебаний карбонильной группы в ИК-спектрах наблюдается при 1747 см -, что гораздо выше, чем для Н Н - дизамещенных амидов. Молекула гетероцикла служит отличной уходящей группой. [35]
Эти реакции отличаются от присоединения RMgX к хлор ангидридам и сложным эфирам кислот, в результате которого образуются неустойчивые аддукты, разлагающиеся до кетонов без помощи кислоты. Разница в стабильности этих аддуктов связана с основными свойствами входящих в их состав элементов. Разложение комплексов в случае хлористого ацила и сложного эфира приводит к кетону и галогениду магния или алкоголяту магния соответственно. Тот же тип разложения комплекса в случае амида должен был бы привести к образованию амида магния, вследствие чего этот процесс оказывается гораздо менее выгодным. Стабильность комплекса амида поэтому достаточно высока, и он способен к существованию до тех пор, пока не будет разрушен добавлением воды и кислоты ( НС1), в результате чего образуется карбонильное соединение и соль амина. Таким образом, реакция 1Ч М - дизамещенных амидов с реактивами Гриньяра ( или, лучше, литийорганическими соединениями) может служить достаточно удобным методом синтеза кетонов. [36]
Страницы: 1 2 3