Алифатические амид
Cтраница 2
 |
Накопление перекисных соединений с ростом дозы облучения N-бутилпропионамида ( 1 и N-бутилбутироамида ( 2 в присутствии кислорода. [16] |
Полярографическим методом в продуктах радиационного окисления алифатических амидов была обнаружена, кроме того, перекись водорода. [17]
 |
Накопление перекисных соединений с ростом дозы облучения N-бутилпропионамида ( 1 и N-бутилбутироамида ( 2 в присутствии кислорода. [18] |
Таким образом, при радиационном окислении алифатических амидов образуются перекиси, карбонильные соединения и спирты, причем образование этих продуктов происходит одновременно и независимым путем. Это указывает на существование параллельных путей превращения радикалов RO2, появляющихся при взаимодействии радикальных продуктов с кислородом. [19]
Если на титрование пропионамида или ЕЫСШИХ первичных алифатических амидов затрачивается слишком много времени, действие гипобромита на бромамид и последующие продукты реакции отразится в понижении поглощения гипобромита и внесет погрешность в окончательный результат. Чтобы предотвратить эти погрешности, гипобромит прибавляют из бюретки достаточно быстро и после достижения конечной точки добавляют еще 3 - 4 порции. Прямая, проходящая через 3 - 4 точки, соответствующие этим порциям титранта, представляет собой вторую ветвь кривой титрования. Для построения первой ветви кривой титрования этих амидов измеряют оптическую плотность свежеприготовленного раствора N-бромпропионамида при 350 нм, рассчитывают молярный коэффициент поглощения его и далее рас-считывают поглощение титруемого раствора в предположении, что N-бромпропионамид образуется точно стехиометрически. Такая первая ветвь калибровочной кривой была использована для определения прошюиамида, бутирамида, валерамида и адипами-да. Вследствие очень небольшого наклона этой начальной части кривой титрования изменения концентрации титруемого амида почти не оказывают влияния на конечный результат, рассчитываемый по данным титрования. [20]
Если на титрование пропионамида или ЕЫСШИХ первичных алифатических амидов затрачивается слишком много времени, действие гипобромита на бромамид и последующие продукты реакции отразится в понижении поглощения гипобромита и внесет погрешность в окончательный результат. Чтобы предотвратить эти погрешности, гипобромит прибавляют из бюретки достаточно быстро и после достижения конечной точки добавляют еще 3 - 4 порции. Прямая, проходящая через 3 - 4 точки, соответствующие этим порциям титранта, представляет собой вторую ветвь кривой титрования. Для построения первой ветви кривой титрования этих амидов измеряют оптическую плотность свежеприготовленного раствора N-бромпропионамида при 350 нм, рассчитывают молярный коэффициент поглощения его и далее рассчитывают поглощение титруемого раствора в предположении, что N-бромпропионамид образуется точно стехиометрически. Такая первая ветвь калибровочной кривой была использована для определения прошюиамида, бутирамида, валерамида и адипами-да. Вследствие очень небольшого наклона этой начальной части кривой титрования изменения концентрации титруемого амида почти не оказывают влияния на конечный результат, рассчитываемый по данным титрования. [21]
Эфиры изоциановой кислоты, полученный из высших алифатических амидов, реагируют с галоидамидами быстрай, чем с водой и щелочью, так что, когда эти амиды подвергаются реакции Гофмана в водной среде, образуются лишь небольшие количества ожидаемых аминов. [22]
 |
Результаты амперометрического титрования первичных амидов раствором гипохлорита кальция. [23] |
Метод с успехом был применен для определения первичных алифатических амидов и ароматических амидов, незамещенных или имеющих только алкильные группы. Наличие других функциональных заместителей в ароматическом кольце вызывает осложнения при определении амидиой группы. [24]
В ряду слабых оснований амиды являются сильнейшими, причем алифатические амиды имеют значения рКа в области 0 0, что соответствует растворам серной кислоты такого интервала концентраций ( 5 - 15 %), где коэффициенты активности и кислотность Я0 претерпевают быстрое изменение. В этой области кислотности концентрация воды все еще достаточна для гидратации ионов, а концентрация электролита быстро изменяется. Поэтому амиды удобно изучать в области концентраций кислоты, промежуточной между концентрациями, пригодными для изучения сильных и слабых оснований. [25]
НОЛЫ - труднее, спирты - Медленно, а алифатические амиды со всем не реагируют с диазометаном. Если реакция метилирования проходит быстро и количественно, как при микросинтезах сложных метиловых эфиров ио, то продукты реакции можно выделять и определять, например, путем газо-жидкостной хроматографии. [26]
Изучение газообразных продуктов радиолиза и радиационного окисления полимера и алифатических амидов позволяет сделать вывод о том, что в процессе облучения происходят разрывы связей С - Н, С-N и С-СО. [27]
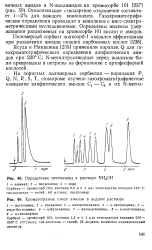 |
Определение метиламина в растворе NH4OH.| Хроматограмма смеси аминов в водном растворе. [28] |
Ясуда и Накашима [239] применяли порапак Q для га-зохроматографического определения алифатических амидов при 230 С; N-метилпроизводные перед анализом были превращены в нитрилы на форколонке с ортофосфорной кислотой. [29]
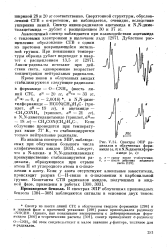 |
Спектры ЭПР радикалов в облученных формамиде ( а, б и 1 Н - диметилформ-амиде ( в, г. [30] |
Страницы: 1 2 3 4