Группа - спирт
Cтраница 2
Последнее свидетельствует о связях между кислородом гидроксилышх групп спиртов, обладающих неподеленными парами электронов, и этими катионами, причем тем большими, чем выше их поляризующая активность. [16]
Какие из следующих соединений не принадлежат к группе изомерных октило-вых спиртов. [17]
Кэмма фракция 4 могла бы быть отнесена к группе спиртов, кислот, альдегидов, кетонов, хинонов, ацетатов, эфиров и ангидридов-лактонов. Во фракциях 5 Б и 5В были найдены фе-вольные и кислые вещества. [18]
Метанол, очевидно, можно отнести ко второй группе спиртов. [19]
Конечно, происходит образование сульфоэфира и по гидро-ксилыюй группе спирта. Таким образом, в молекуле может быть две сульфоэфирных группы и одна сульфогруппа. [20]
Дж / моль ( расчет по сигналу протона НО - группы спирта), тогда как энергия водородной связи с участием протона гидро - пероксида с кислородным атомом спирта составляет - 1О кДж / моль. При взаимодействии гидропероксидов со стабильными радикалами образуются комплексы, что сопровождается уширением сигнала гидроперо-г ксидного протона. [21]
Высокая реакционная способность тозилатов также обусловлена заменой атома водорода в гидрокеильной группе спирта на электроноакцепторную, тозилькую группу. [22]
На этом примере ясно видна зависимость между строением и свойствами ( группа спиртов имеет ряд общих всей группе свойств); определенная группировка атомов вызывает определенные свойства: введение гидроксильной группы в углеводород превращает его в спирт. Таким образом можно говорить о химических функциях, то есть таких группировках, наличие которых влечет появление в молекуле тех или иных характерных свойств, группировках, характеризующих целые классы органических веществ. [23]
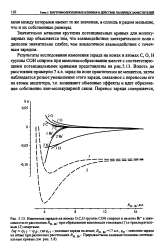 |
Изменения зарядов иа атомах 0С Н группы СОН спиртов и иа ионе Вг - в зависимости от расстояния Ян Вг - при образовании комплексов этиловым ( / и трихлорэтило-вым ( 2 спиртами. [24] |
Результаты исследования изменения заряда на ионах и атомах С, О, Н группы СОН спиртов при комплексообразовании вместе с соответствующими потенциальными кривыми представлены на рис. 5.13. Вплоть до расстояния примерно 7 а.е. заряд на ионе практически не меняется, затем наблюдается резкое уменьшение этого заряда, связанное с переносом его на атомы акцептора, т.е. возникают обменные эффекты и идет образование собственно ион-молекулярной связи. [25]
При добавлении - бутилового спирта к ТБОТ при 20 наблюдаются общие сигналы от протонов указанных выше групп спирта и алко-ксилыюй группы титанита, что свидетельствует о быстром обмене алко-ксильиыми группами между ТБОТ и н-бутиловым спиртом. [26]
Такой механизм реакции подтверждается образованием альдегида и тем, что к ароматическому углероду перемещается водород С - Н - группы спирта. Последнее доказано с помощью меченых атомов. [27]
Наряду с фенолами известно большое количество гидрпксиль-ных производных ароматических углеводородов с гидроксильной группой в боковой цепи - это ароматические спирты, обнаруживающие все признаки группы спиртов. В отличие от фенолов они не растворяются в щелочах, первичные спирты легко окисляются в альдегиды, вторичные в кетоны, образуют простые и сложные эфиры. С крезолами изомерен бензиловый спирт, отличающийся от крезолов положением гидроксильной группы. [28]
С); при более высокой температуре ( 250 - 270 С) гидроксильная группа в момент образования может заместиться водородом, но уже существующие гидроксильные группы спиртов не восстанавливаются. [29]
В табл. 1 - 2 представлены основные спектральные параметры полос поглощения основного тона ( верхняя строчка) и первого обертона ( нижняя строчка) валентных колебаний группы ОН спиртов и группы NH аминов. [30]
Страницы: 1 2 3 4