Группа - галоген
Cтраница 1
Группа галогенов предшествует в периодической системе элементов инертным газам, и их химия определяется тенденцией к достижению электронных конфигураций инертных газов. В этом отношении галогены можно сопоставить с щелочными металлами, хотя по электроотрицательности эти две группы соответствуют двум противоположным предельным случаям. В табл. 85 приведены электроотрицательности, электронные конфигурации и потенциалы ионизации галогенов. [1]
Внутри группы галогенов при переходе от легких к тяжелым элементам наблюдаются не только сходство физических и химических свойств, но и их закономерное изменение. Так, температура плавления и кипения, а также плотность постепенно возрастают, углубляется окраска, уменьшается прочность двухатомных молекул свободных галогенов. Также закономерно изменяются при переходе от фтора к иоду химические свойства, ослабевают окислительные свойства галогенов, падает реакционная способность по отношению к водороду и металлам, но возрастает прочность кислородных соединений, сила галогеноводородных кислот и их восстановительная активность. [2]
В группу галогенов включают элементы: фтор, хлор, бром и йод. Эти элементы сходны по химическим свойствам. [3]
В группе галогенов фтор занимает первое место в VII группе периодической системы, так как его атомный вес наименьший: фтор - 19, хлор-35 5, бром - 80 и йод-127. Фтор является самым активным из всех химических элементов, поэтому в свободном виде в природе он не встречается. [4]
В группе галогенов выделяется ближайший сосед кислорода. [5]
В группе галогенов фтор занимает первое место в периодической системе, так как его атомный вес наименьший: фтор-19, хлор-35 5, бром 80 и иод-127. Фтор самый активный из всех химических элементов, поэтому в свободном виде в природе он не встречается. [6]
В группе галогенов фтор занимает особое место из-за малого размера атома. Мы уже отмечали, что в водном растворе фтор является очень сильным окислителем и что окислительная способность обусловлена в основном большой энергией гидратации иона фтора. Другая характерная особенность фтора заключается в том, что фтористый водород по свойствам отличается от других галогеноводородов. [7]
Сходство элементов группы галогенов основано на сходстве в структуре внешней электронной оболочки: атомы всех галогенов во внешней электронном слое содержат по 7 электронов. В связи с этим все галогены в их соединениях с водородом и металлами отрицательно одновалентны. [8]
Атомам элементов группы галогенов недостает по одному электрону, чтобы приобрести строение атомов инертных газов, кроме того, галогены характеризуются большими значениями ПИ. [9]
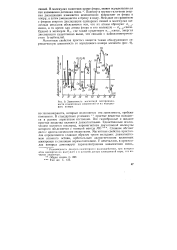 |
Зависимость магнитной восприимчивости гомоатомных соединений от их порядкового номера. [10] |
Поэтому в группе галогенов энергия диссоциации изменяется немонотонно: возрастает от фтора к хлору, а затем уменьшается к брому и иоду. Меньшие по сравнению с фтором энергии диссоциации одинарных связей в молекулах щелочных металлов объясняются тем, что их атомы образуют сг5 5-связи, в то время как атомы фтора в его молекуле - о - связи. Однако в молекуле Н2 где также существует ст, - связь, энергия диссоциации существенно выше, что связано с кайносимметрично-стью ls - орбиталей. [11]
Как в группе галогенов от фтора к иоду меняется агрегатное состояние простых веществ при комнатной температуре. [12]
У элементов VII группы галогенов, кроме фтора, существуют кислоты, в которых атомы галогенов могут находиться во всех нечетных положительных степенях окисления. Степень окисления 5 обозначается с помощью суффикса - новат, 3 - суффикса - ист, 1 - суффикса - новатист. [13]
 |
Некоторые свойства кислорода и его аналогов. [14] |
Как и в группе галогенов, физические и химические свойства рассматриваемых элементов закономерно изменяются с увеличе - нием порядкового номера. Поэтому неметаллические свойства, ярко выраженные у кислорода, оказываются очень ослабленными у теллура. [15]
Страницы: 1 2 3 4