Группа - галоген
Cтраница 3
Как и в группе галогенов, физические и химические свойства рассматриваемых элементов закономерно изменяются с увеличением порядкового номера. Поэтому неметаллические свойства, ярко выраженные у кислорода, оказываются очень ослабленными у теллура. [31]
Получение менее активных элементов группы галогенов химическими методами основывается на различии в их электроотрицательности. Ясно, что фтор дол жен вытеснять хлорид -, бромид - и ио-дид-ионы из их солей, хлор вытесняет бромид-и иодид-ионы, а бром-иодид-ионы. [32]
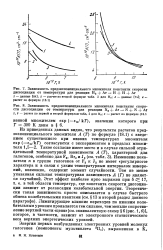
Изменение показателя п в группе галогенов от F2 к J2 не имеет регулярного характера и в связи с узким температурным интервалом измерений, возможно, содержит элемент случайности. Тем не менее указанная сильная температурная зависимость А ( Т) не является случайной. Лимитирующее влияние переходов по нижним колебательным уровням проявляется тем сильнее, чем меньше сопротивление верхней части цепи [ см. эквивалентную схему § 6 ( рис. 1 6) ], которое, в частности, зависит от электронного статистического веса верхних энергетических уровней. [34]
Поэтому электронные эффекты в группе галогенов меняются неправильным образом. В случае менее электроотрицательных заместителей ( - NR2, - OR) индуктивный ( - / ( - эффект меньше и одновременно возрастает способность к ( Л /) - смещению. [35]
В VII группе - группе галогенов, являющихся типичными неметаллами, находится марганец, у которого преобладают металлические свойства. [36]
Иод является наименее распространенным элементом группы галогенов. Он находится в морской воде, в некоторых минеральных источниках и в некоторых редких минералах, особенно в виде иодидов серебра, меди и свинца. [37]
Таким образом, на примере группы галогенов мы можем сделать следующий важный вывод: общность в свойствах элементов одной группы обусловлена одинаковым строением внешней электронной оболочки атомов эле-ментов этой группы, а закономерное изменение свойств ( ослабление неметаллических и усиление металлических) при переходе от легких элементов группы к тяжелым вызывается увеличением числа электронных оболочек и ослаблением связи внешних электронов с ядром при возрастании размеров атомов. [38]
В табл. 14 представлен обзор группы галогенов. [39]
Иод является наименее распространенным элементом группы галогенов. Он находится в морской воде, в некоторых минеральных источниках и в некоторых редких минералах, особенно в виде иодидов серебра, меди и свинца. [40]
В табл. 29 представлен обзор группы галогенов. [41]
Бром и йод относятся к группе галогенов, следовательно, тяк же как хлор, в последнем электронном слое имеют по 7 электронов. Атомы брома и йода легко присоединяют по одному электрону, превращаясь в отрицательно заряженные ионы. Подобно хлору, атомы брома и йода могут и отдавать электроны. [42]
Какие химические элементы относятся к группе галогенов. [43]
Закономерное нарастание неметаллических свойств в группе галогенов сверху вниз проявляется не только в изменении физических свойств простых веществ ( иод - твердое вещество с металлическим блеском), но и их соединений. [44]
Так, например, в группе галогенов фтор является самым сильным окислителем, тогда как иод обладает уже сравнительно невысокой окислительной активностью. Поэтому их называют также окислителями-восстановителями. У неметаллов окислительные свойства выражены сильнее, чем восстановительные. [45]
Страницы: 1 2 3 4