Спиртовая группа
Cтраница 2
Положение спиртовой группы было указано на основании сходства тропина с полученным Фишером триацетоналкамином ( X), миндальный эфир которого, так же как и миндальный эфир тропина ( гоматропин), оказывает на зрачок расширяющее действие - интересный и давно известный случай применения фармакологии в органической химии. [16]
Защита спиртовой группы путем превращения в метиловый эфир имеет ограниченное синтетическое применение из-за низких выходов при последующем расщеплении эфира. [17]
Наличие спиртовых групп в молекулах целлюлозы обусловливает ее высокую реакционную способность. При действии га-логеналкилов или алкилсульфатов образуются простые, а при действии кислот или их ангидридов - сложные эфиры целлюлозы. [18]
Защита спиртовой группы образованием сложного эфира иногда имеет преимущество перед ацетальной защитой, например тетрагидро-пираннлыюй. Обычно ацетали устойчивы к действию оснований и неустойчивы к кислотам, в то время как сложные эфиры в кислой среде более устойчивы, чем ацетали, по - легко гидролизуются в щелочной среде. Сложные эфиры особенно удобны в реакциях окисления, но их нельзя использовать в реакциях с металлорганическими соединениями. В качестве защитных групп чаще всего используют ацетаты и бензоаты; олн легко получаются реакцией незатрудненного спирта с з ксусным ангидридом или хлористым бензоилом в присутствии пиридина или другого третичного амина. [19]
Защита спиртовых групп превращением их в эфирные. [20]
Окисление спиртовых групп в производных моносахаридов по таким схемам широко применяется в синтетической практике. Окисление первично-спиртовой группы служит для синтеза уроновых кислот. [21]
Замещение спиртовой группы на галоген. [22]
Защита спиртовой группы образованием сложного эфира иногда имеет преимущество перед ацетальной защитой, например тетрзгидро-пираннлыюй. Обычно ацетали устойчивы к действию оснований и неустойчивы к кислотам, в то время как сложные эфиры в кислой среде более устойчивы, чем ацетали, но - легко гидролизуются в щелочной среде. Сложные эфиры особенно удобны в реакциях окисления, но их нельзя использовать в реакциях с металлорганическими соединениями. В качестве защитных групп чаще всего используют ацетаты и бензоаты; они легко получаются реакцией незатрудненного спирта с з ксусньш ангидридом или хлористым бензоилом в присутствии пиридина или другого третичного амина. [23]
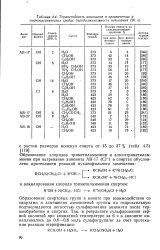 |
Термостойкость анионитдв в органических и водноорганических средах ( продолжительность испытания 120 ч. [24] |
Образование спиртовых групп в ионите при взаимодействии со спиртами и замещении аммониевой группы на гидроксильную подтверждается легкостью сульфирования анионита после термообработки в спиртах. [25]
Метилирование спиртовой группы кодеина диметилсульфатом или йодистым метилом сопровождается алкилированием по азоту и образованием соли четвертичного основания. [26]
Взаимодействие спиртовой группы этиленхлоргидрина с кислотами и их ангидридами, при котором получаются сложные эфиры. [27]
Водород спиртовой группы энольной формы замещается одной валентностью металла, а дополнительной валентностью атом металла связывается с кислородом кетонной группы, образуя ше-стичленное кольцо. [28]
Имея три спиртовые группы, глицерин может вступать в ряд реакций, в которых участвуют один, два или все три гидроксила. [29]
Имея три спиртовые группы, глицерин может вступать в ряд реакций, в которых участвует один, два или все три гидроксила. [30]
Страницы: 1 2 3 4