Вторичная спиртовая группа
Cтраница 1
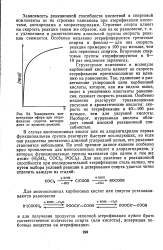 |
Зависимость концентрации эфира при этерификации спиртов ангидридами от времени, реакции. [1] |
Вторичные спиртовые группы этерифицируются в 6 - 10 раз медленнее первичных. [2]
Вторичная спиртовая группа легче теряет гидроксил, чем первичная. [3]
Вторичные спиртовые группы также могут вступать во взаимодействие. [4]
Даже вторичные спиртовые группы могут быть устойчивы к ацилированию, если они находятся в сложных циклических системах, что объясняется влиянием пространственных факторов. [5]
Окисление вторичных спиртовых групп до карбоксильных в одну стадию до настоящего времени не разработано. [6]
Окисление вторичных спиртовых групп макромолекулы целлюлозы раствором йодной кислоты или ее солей производится в водных растворах, в отличие от окисления раствором тетрааце-тата свинца, которое проводится в органических растворителях. Проведение реакции в водных растворах обеспечивает большее набухание целлюлозы и, соответственно, более равномерное протекание реакции. Поэтому для получения препаратов диальде-гндцеллюлозы обычно применяют окисление йодной кислотой, а не тетраацетатом свинца. Введение в элементарное звено макромолекулы целлюлозы двух альдегидных групп в положения 2 и 3 значительно изменяет свойства препаратов. [7]
Преимущественному отщеплению вторичной спиртовой группы, а не третичной гидроксильной группы при Си, может благоприятствовать как стремление к образованию сопряженной системы, так и то, что лишь группа при С - образует ацетильное производное. [8]
Для защиты вторичных спиртовых групп / - сорбозы в дальнейшем процессе окисления / - сорбозы необходимо предварительно провести процесс ацетони-рования. [9]
Эфедрин содержит вторичную спиртовую группу, идентифицированную бензоилированием, и вторичную аминогруппу, легко обнаруживаемую по образованию нитрозамина. [10]
Поливиниловый спирт содержит вторичные спиртовые группы и вступает в реакции, свойственные этим группам, в частности, он взаимодействует с альдегидами с образованием ацеталей. [11]
В случае а-окснальдегндов с вторичной спиртовой группой, однако, образуется с кислой среде кстоспирт не с первичной спиртовой группой, ожидаемый по схеме, а с вторичной [69] группой что ограничивает применимость спиртоокисной схемы по Фаворскому. [12]
Оксикислоты, содержащие первичные или вторичные спиртовые группы, способны за счет последних к реакции окисления. Особенно легко окисляются а-оксикислоты, в которых атом водорода при углеродном атоме в а-положении активирован соседством карбоксильной группы. Так, например, из молочной кислоты при окислении образуется кетопропионовая кислота, называемая пировиноград-ной кислотой ( стр. [13]
Оксиальдегиды жирного ряда, содержащие вторичную спиртовую группу, в тех же условиях в кислоты не превращаются. [14]
Как и в реакции алкилирования, вторичные спиртовые группы в сахарах ацилируются быстрее первичных. Скорость ацили-рования снижается, если гидроксил участвует в образовании водородной связи. [15]
Страницы: 1 2 3 4