Вторичная алкильная группа
Cтраница 2
При диалкилировании малонового эфира введение первичной алкильной группы всегда должно предшествовать введению вторичной алкильной группы. Несоблюдение этой предосторожности приводит к тому, что введение второй алкильной группы часто оказывается безрезультатным [35, 145-149] вследствие низкой кислотности промежуточного продукта - эфира втор-алкилма-лоновой кислоты ( стр. [16]
Катализируемая основанием дегидратация протекает через енолят-анион [ схема ( 60) ], однако если R представляет собой первичную или вторичную алкильную группу, могут происходить дальнейшие катализируемые основанием альдольные конденсации. [17]
 |
Неспособ - из псевдо-я - Мо алкила может ность группы RI в взаимодействовать с р - АО сосед - - CR1R2R3 к сверхсо - него атома углерода. Если одна. [18] |
Теперь, если эффект Бекера - Натана обусловлен отличием в сверхсопряжении с СН и СС, то в случае первичной или вторичной алкильной группы - CH2R или - CHR2 влияние алкила на соседний этиленовый ( sp2) углерод должно изменяться в зависимости от их взаимной ориентации и быть минимальным, когда атом водорода расположен в узловой плоскости соседнего яр2 - атома углерода. [19]
Впоследствии более стойкие алкилаты были получены в результате замены толуола бензолом с использованием для алкилирования полипропилена вместо триизобутилена ( благодаря этому вводилась более стойкая вторичная алкильная группа) и применения более четкого фракционирования конечного продукта. Эти более новые алкилаты напоминают по легкости сульфирования толуол. Однако они отличаются тем, что к ним не применима методика перегонки при парциальном давлении для завершения реакции сульфирования, так как они имеют высокие пределы выкипания и склонность к потемнению и расщеплению, если применяются температуры выше 70, особенно в присутствии серной кислоты. Кроме того, эти углеводороды лишь с трудом образуют полисульфо-кислоты или сульфоны и значительно не расщепляются при обработке их концентрированным олеумом и даже сорным ангидридом, что обеспечивает применение последнего в качестве сульфирующего агента в виде разбавленных газовых смесей. Следовательно, применение таких сильных сульфирующих агентов не только возможно, но и представляется единственным практически применимым методом для достижения полного сульфирования без использования большого избытка кислоты. При применении серного ангидрида фактические выходы приближаются к теоретическим. [20]
По-видимому, лучше применять алкоксиды одновалентной ртути, в частности Hg2 ( OCMe3) 2; в этих реакциях осуществляется перенос двух вторичных алкильных групп. [21]
Алкилирование алкинилтриалкилборатов гладко идет при действии самых разнообразных алкилирующих агентов, причем от бора к а-углероду легко мигрируют как фенильные, так и первичные и вторичные алкильные группы. Таким образом, эта реакция представляет собой общий метод синтеза дизамещенных и триза-мещенных кетонов, причем все операции, от получения органобо-рана до окисления, проводят в одном приборе без его модификации. Единственный недостаток метода в том, что используется только одна из трех алкильных групп у атома бора, и до сих пор не удалось найти такие две группы ( связанные с атомом бора), которые бы не мигрировали и не влияли на ход реакции. [22]
Как и в случае N-нитрозоамидов, образование сложных эфиров является предпочтительным при наличии у азота первичной алкильной группы, а образование алкенов - при наличии вторичной алкильной группы. [23]
Повидимому, характер алкильной группы монозамещенных ацетиленов имеет большое значение в этой реакции, так как ацетиленовые углеводороды, содержащие нормальный алкиль-ный радикал, дают эту реакцию, а ацетиленовые углеводороды с вторичной алкильной группой изомеризуются в диоле-фины. Возможно, что эта изомеризация основана на присоединении и последующем отщеплении элементов спирта. [24]
Патент США, № 4101346, 1978 г. Гидрофобное покрытие на поверхности алюминия можно получить, обрабатывая его в водном растворе щелочи и алифатической карбоновои кислоты с длинной углеводородной цепью ( или карбоксилата), которая содержит одну или несколько коротких вторичных алкильных групп на конце или вблизи неполярного радикала карбоновои кислоты. [25]
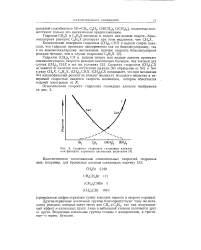 |
Скорость гидролиза галоидных алкилов как функция характера алкильных радикалов. [26] |
Другие первичные алкильные группы благоприятствуют тому же механизму реакции, который имеет место для СН3 и С2Н5, так как индукционный эффект н-алкильных групп лишь в небольшой степени отличается друг от друга. Вторичные алкильные группы сходны с изопропилом, а третичные-с трет, бутилом. [27]
Первичные и вторичные алкильные группы, присоединенные к бензольному кольцу, окисляются до карбоксильной группы. [28]
В этих условиях происходит перенос только двух из трех алкильных групп от бора к углероду; одна группа неизбежно теряется. Поскольку первичные и вторичные алкильные группы мигрируют гораздо легче третичных, для полного использования ценных алкильных групп применяют смешанные органобораны, имеющие теряемую третичную группу. И если учесть, что многие смешанные диалкилтексилбораны легко получить постадий-ным гидроборированием ( см. гл. [29]
При равновесии первично-вторичной или первично-третичной пары изомерных аллильных галогенпроизводных преобладает первичный член. Как и ожидали, вторичная алкильная группа смещает равновесие дальше в сторону первичного изомера. [30]
Страницы: 1 2 3