Альдегидная группа
Cтраница 1
Альдегидные группы защищают переводом в ацетали. Таким путем, по Волю [314], из ацеталя акролеина получается ацеталъ глицеринового альдегида ( см. Синт. [1]
Альдегидная группа гидрируется значительно легче кетонной. Восстановление альдегидов часто можно провести в мягких условиях - при - 50 - 150 С ( с никелем и хромитами) или при 200 - 250 С ( с сульфидами металлов); гидрирование кетонов требует болео жестких условий - соответственно 150 - 250 и 300 - 350 С. [2]
Альдегидная группа гидрируется значительно легче кетонной. Восстановление альдегидов часто можно провести в мягких условиях - при 50 - 150 С ( с никелем и хромитами) или при 200 - 250 С ( с сульфидами металлов); гидрирование кетонов требует более жестких условий - соответственно 150 - 250 и 300 - 350 CL Для ускорения реакции и повышения равновесной степени конверсии процесс ведут под давлением; в интервале 10 - 20 ат с никелевым контактом, при 50 - 200 ат с хромитами и до 300 ат с сульфидами металлов. [3]
Альдегидная группа - типичный электрофильный заместитель; ее сопряжение с бензольным кольцом приводит к понижению электронной плотности в орто - и пара-положениях. [4]
Альдегидная группа вступает ( с хорошей избирательностью) обычно в пара-положение к активирующей группе и лишь затем - в орго-положение, если пара-положение занято. [5]
Альдегидная группа, введенная одним из рассмотренных приемов, вступает преимущественно в пара-положение по отношению к ОН-группе. Если пара-положение занято, то в ряду бензола о-оксиальдегиды получаются с плохими выходами. Для алкильных эфиров фенолов ориентация остается той же ( преимущественно пара -), но при занятом пара-положении получаются орто-продукты. Обычно в ядро входит лишь одна карбонильная группа даже у полиокси - ( и полиалкокси) - замещенных. [6]
Альдегидная группа относится к мета-ориентантам. [7]
Альдегидная группа оказывает активирующее действие, причем, принимая во внимание, что она обладает - /, - Т эффектами, этот факт также представляется неожиданным. Теоретически вполне логично ожидать, что если в этилен вступит достаточно электроотрицательная группа, то его реакционная способность может перейти от нуклеофильной в электрофильную. В этом случае богатый электронами атом углерода будет удерживать свои электроны настолько крепко, что тенденция к обобщению их будет выражена у него лишь в слабой степени; напротив того, электро-ноакцепторный характер бедного электронами углерода будет выражаться вполне отчетливо. [8]
Альдегидная группа умеренно полярна, и этим обусловливается умеренная растворимость альдегидов в воде. [9]
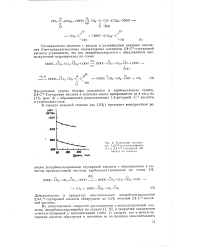 |
Изменение активности 1 2 - С14 - и-кстоглутаровой ( 1 и 2 4 - С14 - глутаровой ( 2 кислот во цремени. [10] |
Альдегидная группа быстро окисляется в карбоксильную группу. С 4 - Глутаровая кислота в условиях опыта превращается за 4 часа на 11 % ( рис. 2) с образованием радиоактивных 1 3-янтарной - См кислоты и углекислого газа. [11]
Альдегидная группа быстро окисляется до кислоты. Возможно, что аналогичный механизм реализуется также для р-кето - или р-гидропероксикислот, с той лишь разницей, что при их распаде образуется дикарбоновая кислота, содержащая на два углеродных атома меньше, и выделяются две молекулы двуокиси углерода. [12]
Альдегидная группа далее окисляется до кислоты. [13]
Альдегидная группа, введенная одним из рассмотренных приемов, вступает преимущественно в пара-положение по отношению к ОН-группе. Если пара-положение занято, то в ряду бензола о-оксиальдегиды получаются с плохими выходами. Для алкильных эфнрон фенолов ориентация остается той же ( преимущественно пара -), но при занятом пара-положении получаются орто-продукты. Обычно в ядро входит лишь одна карбонильная группа даже у полиокси - ( и полна лкокси) - замещенных. [14]
Альдегидная группа образует азометины с первичными ароматическими аминами. [15]
Страницы: 1 2 3 4