Неполярная группа
Cтраница 2
 |
Схема равновесий в водном растворе между натив-ным, мономерным, глобулярным белком, двумя денатурированными состояниями белка ( а и твердым, полимерным и денатурированным состояниями ( б. [16] |
Влияние солей на неполярные группы также не играет решающей роли в этих равновесиях, как это следует из отсутствия корреляции между эффектами различных солей с известными константами высаливания модельных неполярных неэлектролитов. [17]
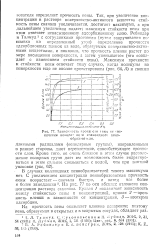 |
Зависимость прочн - сти i ены от vse. [18] |
Длинными радикалами ( неполярные группы), направленными в разные стороны, дают переплетение, способствующее прочности слоя. [19]
Переносчик должен содержать полярные и неполярные группы. [20]
В случае замены неполярной группы на полярную межмолекулярное взаимодействие усиливается и подвижность звеньев уменьшается; в результате время релаксации процессов дипольно-сегмен-тального типа увеличивается. Замещение СН3 - группы на конце бокового радикала хлором повышает время релаксации, что связано с возрастанием полярности полимера. [21]
Связи между этими неполярными группами являются слабым местом мультимолекулярного слоя, сформированного из молекул жирных кислот и других им подобных полярно активных молекул, имеющих строение в виде открытых цепочек. [22]
На преодоление энергии связи неполярных групп молекул, в результате которой происходит сближение отдельных мицелл во время процесса застудневания. [23]
Если в поверхностный слой входят полярные и неполярные группы, то картина резко усложняется, однако для широкого обобщения данных недостаточно. [24]
В адсорбционных пленках происходит ассоциация неполярных групп. Строение адсорбционного слоя зависит от природы ПАВ и межфазной поверхности, степени заполнения поверхности, введения в среду различных добавок. Изменение строения адсорбционного слоя отражается на его защитных свойствах. [25]
Молекулы поверхностно-активных веществ состоят из полярных и неполярных групп. Полярные группы-это ОН, СООН, NH2, SO3H и другие, а неполярные-это углеводородные цепи: прямые, разветвленные, замкнутые или их сочетание. Такая двойственность в структуре и определяет поведение молекул ПАВ в растворе и на границе раздела фаз. [26]
Связи третьего типа возникают между неполярными группами. На это указывают низкие точки плавления и точки кипения низших членов парафинового ряда. Взаимное притяжение между неполярными группами, которое может быть эффективно только между большими, протяженными группами, например длинными парафиновыми цепями высших жирных кислот, усиливается благодаря способности насыщенных парафиновых цепей деформироваться. Парафиновые цепи в связи с тем, что их атомы углерода могут свободно вращаться вокруг связи углерод - углерод, обладают большой гибкостью и могут поэтому сближаться одна с другой достаточно близко, чтобы силы притяжения эффективно вступили в действие. [27]
В тех случаях, когда варьируются неполярные группы, расположенные достаточно далеко от радикального фрагмента, как, например, в случае радикалов АХ ( ге), изменения величин а не наблюдается ( см. табл. 1.3), что свидетельствует об отсутствии искажения в строении радикального фрагмента. Линейная зависимость между величинами а и дипольными моментами заместителей, наблюдаемая для таких радикалов ( см. рис. 1.4), обусловлена прямым электростатическим взаимодействием: полярный заместитель непосредственно на радикальном фрагменте создает. Если взаимодействие радикального фрагмента с полем смещает равновесие в схеме валентных структур (1.10), например, в пользу структуры А, то это приводит к уменьшению величины pN, а тем самым и к уменьшению величины а. [28]
Если молекулы одной из жидкостей содержат одновременно полярные и неполярные группы ( например, спирты, амины, органические кислоты), они способны ориентироваться в поверхностном слое полярной группой в сторону более иолярнои фазы. В этом случае правило Антонова не соблюдается, поскольку строение поверхностного слоя не отражает строения фазы. [29]
Эти функциональные полярные группы отличаются от неполярных групп химических веществ тем, что они способны образовывать ионы и нести на себе определенный электрический заряд. [30]
Страницы: 1 2 3 4