Восстанавливающаяся группа
Cтраница 2
Амины, растворимые в щелочных растворах, оса ждают уксусной кислотой Этот метод дает превосход ньге результаты при восстановлении ароматических нитрокарбоновых кислот Большим преимуществом этого метода является возможность восстановления нитро-группы при наличии в соединении других легко восстанавливающихся групп без их разрушения. [16]
Исходя из вышесказанного, по-видимому, можно сделать вывод [14], что для восстановления карбоксигруппы до альдегидной необходимо соблюдение следующих условии: 1) карбоксн-группа должна быть активирована сильной злектроноакцепгор-ной группой; 2) карбоксигруппа должна быть наиболее легко восстанавливающейся группой в молекуле ( что автоматически исключает присутствие в качестве активирующих групп нитро-группы и некоторых азотсодержащих гетероароматнческих групп); 3) дальнейшему восстановлению образующегося альдегида должно препятствовать образование из него иевосстанав-ливающегося соединения, например гидрата или полуацеталя. [17]
Этот реагент рекомендуется для образцов, содержащих восстанавливающиеся группы. [18]
Удельная емкость органического окислителя повышается при увеличении в его составе количества восстанавливающихся групп: - NOa в нитросоединениях и - NO в нитрозосоединениях, что повышает также и разрядный потенциал электрода. Последний, кроме того, зависит от взаимного расположения восстанавливающихся групп. Процесс восстановления нескольких таких групп может протекать стадийно, следствием чего является ступенчатость разрядной кривой электрода. Значительное влияние на потенциал электрода оказывает наличие в окислителе других введенных групп. Соединения, содержащие электронопритя-гивающие группы, такие как - fNO2, - CN, - СНО и - CONH2, восстанавливаются при более положительном потенциале, тогда как наличие в веществе электроноотталкивающих групп, таких как - NH2, - NCCzHs), - СНз, - ON, вызывает сдвиг потенциала в отрицательную сторону. Влияние введенных радикалов рассматривается с точки зрения воздействия их на электронную плотность вокруг восстанавливающейся группы. Последнее выражается в сдвиге потенциала восстановления ( в конкретном случае - разряда) в более положительную сторону. Обратное влияние отмечается для случая электроноотталкивающих радикалов. Степень воздействия инертных радикалов зависит от их расположения в структурной формуле веществ по отношению к восстанавливающейся группе. [19]
Эти гидридьи реагируют аначогично литийалюминийгид-риду. Наименее активным среди них является магний-ал юмииийгнчрид, который реагирует только с чегко восстанавливающимися группами, аимсшюскарбшшль - РЫМН, карбоксильными, эфирными, амидныкми н ни-трилышми [33, 266] Этот реагент не действует на иитро-группы, гачоиды и двойные с-вячи Активность ачюмо-гидридов натрия и кальцин приблизительно та же, что и Li lH j Натрнйалюминийгидрид исследован лучше тру-гих Он ие растворяется в сложном эфире, и при восстановлении применяют его раствор в теарагндрофуранс. [20]
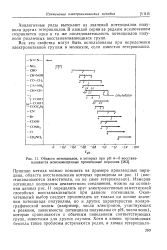 |
Области потенциалов, в которых при рН 4 - 5 восстанавливаются монозамещенные производные пиридина. [21] |
Аналогичные ряды вытекают из значений потенциалов полуволн других гетероциклов. В каждой серии за редким исключением сохраняется одна и та же последовательность потенциалов полуволн различных восстанавливающихся групп. [22]
Как указывалось выше, 11-кетогруппа в ряду стероидов и три-терпенов сильно затруднена и при восстановлении литийалюми-нийгидридом дает аксиальный спирт. Этот метод восстановления широко применяется при исследовании природных соединений, и единственным практическим ограничением его применимости является наличие в молекуле других восстанавливающихся групп, что может усложнить интерпретацию результатов. [23]
Предложенное уравнение нуждается в дальнейшей проверке и теоретическом обосновании с позиций современной теории растворов. Следует указать, что еще в работах [42, 43] был сделан вывод о наличии параллелизма между легкостью электровосстановления и величиной собственного дипольного момента восстанавливающейся группы. Вероятно, собственный дипольный момент электроактивной группы в ряде случаев может меняться и в зависимости от селективной сольватации данной группы молекулами растворителя, однако количественная оценка данного эффекта не проста и даже в пределах одной изоструктурной и гомологической серии перераспределение электронной плотности для различных представителей серии под влиянием растворителя может проявиться по-разному. [24]
Особенность гидрирования как синтетического метода заключается в применении для восстановления веществ разных классов одного и того же восстановителя и общих или химически родственных катализаторов. Эта особенность ограничивает возможность избирательного гидрирования соединений, если необходимо, например, обеспечить заданную глубину восстановления группы, способной к более глубокому восстановлению, или прогидрировать одну из нескольких восстанавливающихся групп, не затрагивая остальных. [25]
Получены макроциклические амиды, содержащие бутильный, ал-лильный, бензильный, ( 3-гидрокси - и ( 3-цианэтильные радикалы. Если в состав радикала R входят восстанавливающиеся группы, то они также восстанавливаются: Р - ЦИЗНЭТНЛЬНЫЙ радикал восстанавливается до у-аминопропиль-ного. [26]
Гидрогенолиз связи С-галоген является важным методом дега-логенирования органических соединений. Реакция протекает легко на различных катализаторах. Поэтому прогидрировать ненасыщенные функции в галогеносодержащем субстрате и при этом избежать потери галогена нередко не менее сложно, чем удалить атом галогена, сохранив неизменными другие восстанавливающиеся группы. Решающее значение в каждом конкретном случае имеет характер связи С-галоген ( тип галогенопроизводного) и условия реакции, в первую очередь температура. [27]
Диарил - и диалкилдисульфиды восстанавливаются алюмогидридом лития с высоким выходом, однако применение этого восстановителя ограничено пространственными затруднениями вокруг связи S-S. Для восстановления дисульфидов используют также различные системы металл - донор протона: олово, цинк или алюминий и кислота, натрий во влажном эфире, различные амальгамы в сочетании с водой или разбавленной кислотой. Для предотвращения восстановления имеющихся в молекуле дисульфида других восстанавливающихся групп в качестве восстановителя используют глюкозу в щелочном растворе, а также тиолят-ион. [28]
Однако, к счастью, эти затруднения не являются непреодолимыми. Гидроборирование двойной или тройной углерод-углеродной связи протекает настолько быстро, что часто с прекрасным выходом могут быть получены органобораны в присутствии таких функций, как хлорангидридная, сложноэфирная или нитрогруппа. В некоторых случаях допустимо даже наличие такой очень быстро восстанавливающейся группы, как карбоксильная. [29]
Однако, к счастью, эти затруднения не ннлиются непреодолимыми. Гидроборирование двойной или тройной углсрод-углеродлой связи протекает настолько быстро, что часто с прекрасным выходом могут быть получены органобораны в присутствии таких функций, как хлорангидридпая, сложноэфирная или нитрогруппа. В некоторых случаях допустимо даже наличие такой очень быстро восстанавливающейся группы, как карбоксильная. [30]
Страницы: 1 2 3