Гидро-ксильная группа
Cтраница 1
Гидро-ксильная группа часто бывает связана водородной связью с двумя другими гидроксиль-ными группами различных молекул. Кристаллическую структуру можно в таком случае рассматривать как каркас из линий ( связывающих гидроксильные группы), три из которых всегда встречаются в одной точке. [2]
Гидро-ксильные группы в структуре e - Zn ( OH) 2 не свободны, а связаны водородными связями [29], что подтверждается также ИК-спектра-ми поглощения. [3]
Гидро-ксильные группы, далее, этерифицируются серной кислотой. [4]
Гидро-ксильные группы в структуре e - Zn ( OH) 2 не свободны, а связаны водородными связями [29], что подтверждается также ИК-спектра-ми поглощения. [5]
Гидро-ксильная группа, естественно, не имеет частоты 5 ( Н2О), поскольку уже нет угла НОН. В зависимости от природы атома металла М и прочности связи М - ОН эти частоты могут изменяться, оставаясь приблизительно в указанном интервале. Частоты валентных колебаний v ( OH) гидроксильных групп ( как внутрисферных, так и внешнесферных) часто выше частот v ( OH) молекул воды, а соответствующие полосы поглощения нередко более узкие и резкие, чем полосы поглощения воды. [6]
Благоприятно расположенные гидро-ксильные группы образуют устойчивые боратные комплексы, что соответствует высоким значениям MG. Наиболее прочные комплексы образуют г ис-1 2-диолы пятичленных циклов. [7]
Гидро-ксильные группы поверхности стекла могут образовывать с указанными мономерами химические и водородные связи, а также возможно взаимодействие силикатного стекла с полимерным соединением, образующимся в ходе конденсации исходных мономеров на его поверхности. [8]
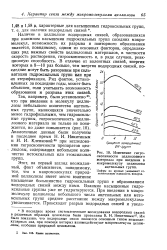 |
Изменение гигроскопичности целлюлозного материала при введении в. [9] |
Взаимно насыщенные гидро-ксильные группы уже не гидратируются. При введении в макромолекулу целлюлозы небольшого числа ацетильных или метоксильных групп среднее расстояние между макромолекулами увеличивается. [10]
Эта гидро-ксильная группа в молекуле исходного стрептомицина была связана с остатком стрептобиозамина и не могла пробензоилироваться при действии на стрептомицин бензоилхлоридом. При последующем же гидролизе полученного бензоильного произвольного стрептомицина произошло отщепление остатка стрептобиозамина, в результате чего и возникла эта гидроксильная группа. Таким образом, дальнейшие исследования должны были свестись к доказательству положения этой гидроксильной группы в молекуле выделенного гепта-бензоилстрептидина, так как тем самым могло быть выяснено и место присоединения остатка стрептобиозамина к стрептидину. С этой целью гептабензоилстрептидин был превращен через соответствующее иодпроизводное в гептабензоил-дезоксистрептидин и далее в Н М - дибензоил-дезоксистрептамин. Последний же оказался способным восстанавливать 1 моль йодной кислоты, откуда следует, что в его молекуле содержатся две гидроксильные группы, расположенные у соседних атомов углерода. [11]
Конфигурация гидро-ксильной группы в а-положении и здесь определяет знак оптического вращения. Все такие соединения, а-оксигруппа которых в фишеровской проекции ( Г, рис. 6 - 25) находится справа, являются правовращающими. Исходя из принципа оптической суперпозиции, Хадсон [ 1231 показал, что преобладающий вклад а-поло-жения в оптическое вращение изменяется под влиянием вкладов от ( 5 - и у-положений. Более подробное изучение оптического вращения таких амидов с учетом тонкой конформационной структуры может принести весьма ценные результаты. [12]
Замещение гидро-ксильных групп фтором не может вызывать сомнения, так как инфракрасной спектроскопией ( ИКС) показано, что обработка фтористоводородной кислотой значительно уменьшает полосы поглощения валентных колебаний гидроксильных групп поверхности. [13]
Взаимодействие гидро-ксильных групп поверхности кремнезема с молекулами воды и спиртов. [14]
По числу гидро-ксильных групп в молекуле различают С. [15]
Страницы: 1 2 3 4