Гидроксильная группа - поверхность
Cтраница 1
Гидроксильные группы па поверхности твердых поликремне-кпслот определяют их сорбцнонные, химические, ионообменные и каталитические свойства. Незавершенность электронной - оболочки кремния вызывает такое распределение электронной плотности в силанольных группах, что отрицательный заряд сильно смещен к атому кислорода. Повышенная подвижность атома водорода ОН-групп является причиной сильного взаимодействия поверхности с молекулами адсорбатов, электронная плотность в которых сосредоточена на периферии, например с полярными молекулами воды, спиртов и др. В водных растворах поверхность силикагеля проявляет слабокислые свойства, поэтому возможно замещение водорода SiOH-rpynn на катионы различных металлов. [1]
 |
Спектр карбонильных групп поливинилацетата, адсорбированного из растворов в СНС13 на аэросиле, откачанном при 400 С в течение 6 час. [2] |
Об участии гидроксильных групп поверхности аэросила во взаимодействии с карбонильными группами макромолекул ПВА свидетельствует изменение их спектра при адсорбции. При переходе к большим величинам адсорбции ( до а 48 мг / г) доля связанных карбонильных групп ПВА несколько уменьшается. Использование в качестве растворителя ССЦ уменьшает долю связанных сегментов. Считается [95], что это связано с тем, что при большей величине адсорбции и меньшей растворимости полимера при наличии одного и того же числа адсорбционных центров на поверхности аэросила может происходить образование более рыхлых клубков макромолекул с меньшим числом карбонильных групп, связанных с поверхностью водородной связью. [3]
Хлор замещает часть гидроксильных групп поверхности и катион алюминия оказывается связанным с двумя различными анионами. [4]
В силу стерических препятствий не все гидроксильные группы поверхности могут быть вовлечены в эту реакцию. Из спектрограмм, приведенных на рис. 39, следует, что обмен поверхностных гидроксильных групп ОН на OD в атмосфере пара D2O, за исключением групп ОН, блокированных у мест контакта глобул и внутри глобул аэросила, у исходного немодифицированного образца происходит полностью. Гидроксильные группы, оставшиеся на поверхности после модифицирования между привитыми триметилсилильными группами, обмениваются медленно и в значительно меньшей степени. [5]
Получаемые в этом случае значения доли гидроксильных групп поверхности, участвующих во взаимодействии с адсорбирующимися молекулами, наиболее близки к получаемым из прямых адсорбционных измерений при том же давлении пара и температуре. [6]
 |
Зависимость частот нормальных колебаний молекулы ацетонитрила от значений силовых постоянных KQl, Kgz и. [7] |
Таким образом, хотя изменение спектра гидроксильных групп поверхности аэросила и указывает на образование водородной связи с адсорбирующимися молекулами, влияние этой связи на частоты колебаний CN ацетонитрила и акрилонитрила меньше, чем в случае синильной кислоты. Объясняется это, по-видимому, уже отмеченной выше нехарактеристичностью колебания CN в молекулах ацетонитрила и акрилонитрила, в результате чего возмущение через атом азота вызывает изменение колебаний всего структурного элемента С - CN этих молекул. [8]
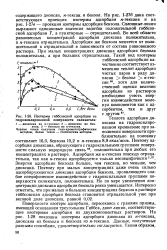 |
Изотермы гиббсовской адсорбции на гидроксилированной поверхности силикагеля. [9] |
Поэтому адсорбция диоаксана, образующего с гидроксильными группами поверхности сильную водородную связь 66, положительна при любых его концентрациях в растворе. Энергия адсорбции бензола больше, чем гексана, но меньше, чем диоксана. Поэтому при малых концентрациях даже очень сильно адсорбирующегося диоксана адсорбция бензола, проявляющего слабое специфическое взаимодействие с гидроксильными группами поверхности силикагеля, положительна. Но по мере увеличения концентрации диоксана адсорбция бензола резко уменьшается. [10]
Взаимодействие функциональных групп молекул адсорбата с гидроксильными группами поверхности адсорбента увеличивает энергию адсорбции молекул, имеющих дипольные и квадруполь-ные моменты или я-электронные связи, и мало изменяет энергию адсорбции молекул с симметричными электронными оболочками. Следовательно, если удалить с поверхности адсорбента гидроксильные группы, то снизится адсорбция адсорбата, молекулы которого имеют дипольные и квадрупольные моменты или л-электронные связи, и мало изменится активность адсорбента для соединений с симметричными электронными оболочками. [11]
Взаимодействие функциональных групп молекул адсорбата с гидроксильными группами поверхности адсорбента увеличивает энергию адсорбции молекул, имеющих дипольные и квадруполь-ные моменты или я-электронные связи, и мало изменяет энергию адсорбции молекул с симметричными электронными оболочками. Следовательно, если удалить с поверхности адсорбента гидроксильные группы, то снизится адсорбция адсорбата, молекулы которого имеют дипольные и квадрупольные моменты или я-электронные связи, и мало изменится активность адсорбента для соединений с симметричными электронными оболочками. [12]
Большую роль часто играет и образование водородной связи между гидроксильными группами поверхности адсорбента и молекулами адсорбтива. [13]
Образовавшиеся при этом алкилсилоксанолы в процессе гидрофобизации реагируют с гидроксильными группами поверхности материала, а также вступают в реакцию поликонденсации. В результате этих превращений на поверхности материала, обработанного алкилсиликонатами натрия, образуется нерастворимая водоотталкивающая пленка RSiOi. [14]
Вместе с тем, в соответствии с рис. 3.23, сами гидроксильные группы поверхности чистого кремнезема не столь активны и образуют лишь водородные связи. Дегидроксилирование чистой поверхности кремнезема, уменьшая ее специфичность, лишь сокращает время удерживания таких молекул и мало влияет на удерживание молекул группы А. [15]
Страницы: 1 2 3 4