Гидроксильная группа - поверхность
Cтраница 2
На этом основании сделано предположение о том, что кислотность гидроксильных групп поверхности достаточна для инициирования реакции конденсации между двумя молекулами ацетальдегида. [16]
Высокочастотная полоса поглощения была приписана валентным колебаниям кислород - водород гидроксильных групп поверхности, а полоса поглощения при 1610 еж 1 - деформационным колебаниям соответствующих гидроксильных групп. Характеристическая полоса поглощения валентных колебаний S - Н к-тиогексана исчезла при его адсорбции. Однако интенсивные полосы поглощения валентных колебаний С - Н в спектре показывали, что углеводородные радикалы присутствуют на поверхности в достаточно высокой концентрации. [17]
Адсорбция молекул воды в основном обусловлена образованием водородных связей с гидроксильными группами поверхности. [18]
Для анализа веществ, способных к сильному специфическому взаимодействию с гидроксильными группами поверхности силика-гелей или пористых стекол, можно использовать графитирован-ные сажи или химически модифицированные силикагели. [20]
 |
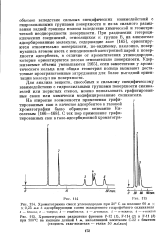
Инфракрасный спектр кремнезема. [21] |
В инфракрасном спектре это проявляется в виде смещения частоты валентных колебаний гидроксильных групп поверхности в более длинноволновую область. Из рис. XVIII, 11 видно, что это смещение Av при неспецифической адсорбции, например при адсорбции насыщенного углеводорода н-гексана, невелико. [22]
Поэтому при сопоставлении изменений частот и интенсивно-стей полосы поглощения валентных колебаний гидроксильных групп поверхности с энергией специфического взаимодействия более правильно из измеряемой суммарной теплоты адсорбции выделить ту ее часть, которая характерна в основном именно для специфического взаимодействия с гидроксильными группами поверхности. Этому больше соответствует отнесение теплоты адсорбции к площади os того звена молекулы, которое взаимодействует с гидроксильными группами поверхности специфически. В соответствии с этим величина ю8 для алкилбензолов приближенно принята такой же, как и для бензола ( сот 40 А2), а для спиртов, воды и эфира величина и8 была принята равной ат для подобных молекул наименьших размеров - воды и метанола. [23]
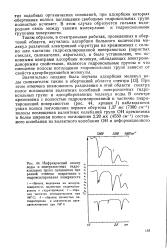 |
Инфракрасный спектр воды и поверхностных гидро. [24] |
В этом случае образуется сильная водородная связь между такими молекулами и гидроксильными группами поверхности. [25]
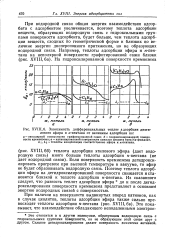 |
Зависимость дифференциальных теплот адсорбции диэти-лового эфира и н-пентана от величины адсорбции на. [26] |
Это относится и к другим молекулам, образующим водородную связь с гидроксильными группами поверхности, но не образующим этой связи друг с другом. Сильное дегидроксилирование делает поверхность химически активной. [27]
 |
Зависимость дифференциальных теплот адсорбции диэти-лового эфира и н-пентана от величины адсорбции на. [28] |
Это относится и к другим молекулам, образующим водородную связь с гидроксильными группами поверхности, но не образующим этой связи друг с - другом. Сильное дегидроксилирование делает поверхность химически активной. [29]
Физическая адсорбция протекает на носителе из кремнезема с образованием водородных свзей между гидроксильными группами поверхности и гидроксилом спирта. Однако все полосы, подтверждающие этот тип адсорбции, исчезли после вакуумирования образца при 20 в течение 30 мин. [30]
Страницы: 1 2 3 4