Поверхностная гидроксильная группа
Cтраница 3
Изменение смещения полосы поглощения поверхностных гидроксильных групп кремнезема AVOH с ростом поверхностной концентрации адсорбированных молекул было объяснено [19] различным изменением с ростом заполнения вкладов энергии специфического и неспецифического взаимодействия в общую энергию адсорбции при разных заполнениях. Так, если бы адсорбирующиеся молекулы занимали вначале наиболее выгодные положения для сильного специфического взаимодействия с гидроксильными группами поверхности, а затем, по мере роста заполнения, все менее выгодные положения, то величина AVOH должна была бы уменьшаться, а не увеличиваться. Однако положение молекулы на поверхности определяется минимумом суммарной энергии ее взаимодействия с адсорбентом. Энергия локального специфического взаимодействия адсорбирующихся молекул с гидроксильными группами поверхности кремнезема составляет важный, но для больших молекул часто лишь относительно небольшой вклад в общую энергию адсорбции. [31]
Он приписал эту полосу поверхностным гидроксильным группам, связанным водородной связью друг с другом н недоступным для реакции с молекулами метанола. На рис. 102 представлен спектр, снятый после адсорбции воды на метилированном стекле. [32]
Показано, что полное замещение поверхностных гидроксильных групп происходит, если силикагель предварительно дегидроксилировать при 500 - 800 С. Однако замечено, что на этих модифицированных силикаге-лях возможны поверхностные химические реакции с участием напряженных силоксановых мостиков силикагеля. [33]
В настоящем разделе обсуждается роль поверхностных гидроксильных групп в адсорбции молекул на поверхности. Кроме того, проведено сравнение относительного вклада свободных и связанных взаимной водородной связью гидроксильных групп в процессах адсорбции и выяснено влияние дегидроксилирования на адсорбционные свойства поверхностей. При этом большое внимание уделено адсорбции воды на гидроксилированных и дегидро-ксилированных поверхностях. [34]
В результате становится возможным взаимодействие поверхностных гидроксильных групп с образованием химических связей, что и обусловливает необратимость изменений величины поверхности высушенных образцов. При этом возможны два случая: размер первичных частиц может остаться неизменным, как это наблюдалось в работе Киселева и соавт. [35]
Хлорирование поверхности аэросила путем реакции поверхностных гидроксильных групп с ВС13 [82] уже рассмотрена выше. [36]
По мнению Лоу и Рамасубраманиана [56] поверхностные гидроксильные группы, связанные с атомом бора, могут быть причиной появления узкой полосы поглощения 3700 смг1 в спектре фторированного пористого стекла, обработанного аммиаком. [37]
При этом образуются гидрид натрия и поверхностные гидроксильные группы. Для объяснения такого явления в работе [66] предположили, что происходит неполный разрыв Н - Н - связи. Остается только объяснить, почему реакции такого типа протекают на Na-морденитах, но не на. [38]
Теренин [10] считает, что взаимодействие поверхностной гидроксильной группы с адсорбированной молекулой приводит к симметризации ее потенциальной кривой. [39]
В частности, была обсуждена роль поверхностных гидроксильных групп н адсорбированной воды в проявлении адсорбционных свойств этих веществ. Было показано, что с поверхности алюмосиликат-ных катализаторов крекинга и каолинита поверхностные гидро-ксильные группы удаляются легче, чем с поверхности силика-геля. Для достижения того же состояния дегидроксилирования силикагелей необходима более высокая температура. Было найдено, что на алюмосиликатах, прокаленных при 300, адсорбировано больше воды, чем на обработанных таким же способом образцах кремнезема. В случае набухающих решеток монтмориллонита и вермикулита это может быть обусловлено способностью межслоевых обменных катионов к сильной координации молекул воды. [40]
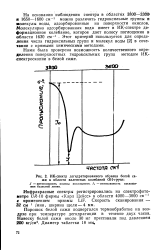 |
ИК-спектр дегидратированного образца белой сажи в области валентных колебаний ОН-групл. [41] |
Нами была проверена возможность количественного определения поверхностных гидроксильных групп методом ИК-спектроскопии в белой саже. [42]
Если расстояние между адсорбированной молекулой и поверхностной гидроксильной группой слишком велико, перенос протона оказывается невозможным, и взаимодействие оставалось аналогичным взаимодействию с льюисовским кислотным центром. [43]
Однако возможна различная прочность связи с поверхностными гидроксильными группами кремнезема в зависимости от их концентрации и ориентации на поверхности. В частности, в работах [16, 17] считается, что центрами адсорбции более прочно-связанных молекул воды могут являться места с повышенным адсорбционным потенциалом на поверхности и у мест контакта глобул спрессованного порошка кремнезема. [44]
При адсорбции наблюдается уменьшение интенсивности полосы поглощения поверхностных гидроксильных групп и появление новых полос поглощения валентных колебаний групп ОН 3390, 3525 и 3640 см-1 и валентных колебаний групп OD 2852 и 2956 см-1. Положение полос поглощения 3390 см-1 близко к положению соответствующей полосы поглощения 3350 см-1 жидкого метанола и соответствует молекулам в капиллярно сконденсированной фазе. Эта полоса поглощения удаляется из спектра после откачки образца при 20 С. [45]
Страницы: 1 2 3 4 5