Имидазольная группа
Cтраница 4
 |
Равновесие между Zn2 и сывороточным альбумином37. [46] |
Значения ( & ха) м были вычислены из соотношения, эквивалентного уравнению ( 31 - 6), в предположении, что имидазольные группы белковой макромолекулы являются единственными реагирующими участками. [47]
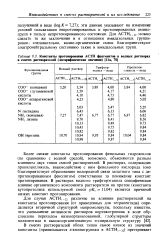 |
Константы протежирования АСТН фрагментов в водных растворах и смесях растворителей ( логарифмические значения [ На, 70 ]. [48] |
Для ACTHi 32 можно сделать те же заключения и в отношении имидазольных группировок; следовательно, водно-органические смеси благоприятствуют электронейтральному состоянию также и имидазольных групп. [49]
Мы предположили [9, 10], что при гидролизе эфира, катализируемого как трипсином, так и химотрипсином, стадия, лимитирующая скорость, зависит от имидазольной группы в ее основной форме в молекуле фермента. [50]
В другом объяснении зависимости / Скаж от кислотности уходящей группы вместо промежуточного тетраэдрического соединения в схеме ( 1 - 193) допускается невалентное взаимодействие ионизированных имидазольных групп с замещенным фенолом пли карбонильным углеродом. [51]
В первоначально предложенной модели было лишь две кинетически различимые стадии: быстрая первоначальная адсорбция субстрата на активном центре фермента и последующее определяющее скорость воздействие имидазольной группы каталитического центра на углерод карбонильной группы субстрата. Эта модель имеет некоторые недостатки, но их можно устранить, если результаты недавних опытов рассмотреть с точки зрения приведенной выше схемы. [52]
В результате исследования [370-373 ] строения активного центра рибонуклеазы ( РНК-азы) поджелудочной железы быка было показано, что в состав активного центра этого фермента входят две имидазольные группы, одна из которых протонирована, а другая находится в виде основания. Другое имидазольное кольцо ( II), находящееся в протонированном состоянии, образует водородную связь с эфирным кислородом. Участок ( III) соответствует области дополнительных связей между ферментом и молекулой нуклеофильного реагента. Таким образом, в переходном состоянии ( см. рис. 26, Б), no - существу, имеет место пуш-пульный механизм, когда нуклео-фильная атака на атом фосфора кислородом активированной окси-группы нуклеофильного реагента сопряжена с образованием водородной связи между кислородом отходящей группировки и кислотной группой фермента. На рис. 26, В показан комплекс фермент продукты. [53]
В то время как гидролиз амидов и алкиловых эфиров химотрипсином характеризуется большими скоростями, гидролиз метилового эфира - ( 4 -имида-золил) масляной кислоты протекает без участия имидазольной группы. [54]
 |
Необратимое ингибирование. [55] |
Другой необратимый ингибитор некоторых ферментов, иодацетамид ( рис. 9 - 11), может взаимодействовать с сульф-гидрильными ( - SH) группами остатков цистеина или с имидазольными группами остатков гистидина, содержащихся в активных центрах этих ферментов. С помощью таких ингибиторов было установлено, что гидроксильная группа серина, тиоловая группа цистеина и имидазольная группа гистидина участвуют в каталитической активности ферментов, принадлежащих к разным классам. [56]
На основании этих, а также и некоторых других косвенных данных первоначально Уилсоном, а затем и другими авторами была высказана мысль о прямом участии в каталитическом действии холинстераз имидазольной группы гистидина, характеризующейся значением рК 5 6 - 7 0 ( см. на стр. Вопрос об идентификации кислотной группировки менее ясен. [57]
Страницы: 1 2 3 4