Парциальное давление - окись - углерод
Cтраница 1
Парциальное давление окиси углерода у внешней поверхности гранулы предположительно равно нулю. Принимается, что азот, содержащийся в исходной смеси, не влияет на ход реакции. Поэтому концентрация азота не фигурирует в уравнении скорости. [1]
Поскольку парциальное давление окиси углерода и водорода над реакционной жидкостью практически остается постоянным, то скорость реакции карбонилирования определяется концентрацией пентена в зоне реакции и формально подчиняется уравнению мономолекулярной реакции. [2]
Повышение парциального давления окиси углерода до определенного предела вызывает увеличение скорости реакции гидроформилирования гексена. [3]
Повышение парциального давления окиси углерода выше определенного предела вызывает замедление реакции гидроформилирования, а повышение парциального давления водорода приводит к ускорению реакции. [4]
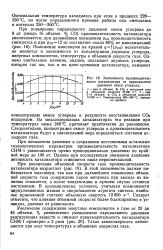 |
Зависимость производительности катализатора от парциального давления окиси углерода. [5] |
При повышении парциального давления окиси углерода до 8 ат ( около 16 объемн. Положение максимума на кривой qf ( pco) незначительно меняется в зависимости от концентрации двуокиси углерода, инертных компонентов, температуры и объемной скорости газа. [6]
При повышении парциального давления окиси углерода скорость абсорбции СО также увеличивается. Поэтому абсорбцию СО производят под давлением 120, 200, 320 атм, а иногда и выше. Из рисунка видно, что очистку газа от СО наиболее целесообразно вести при темиературе порядка 0 - 20, а на выходе из скруббера раствор должен иметь температуру не более 33 - 35 С. Для регенерации раствора его дросселируют до 1 - 2 атм и нагревают до 78 - 79 С. При этой температуре и атмосферном давлении аммиачный комплекс разлагается с выделением окиси углерода. После аммиачно-медных скрубберов газ поступает на окончательную очистку от СО3 и HsS, которая осуществляется 7 - 10-процентным раствором едкого натра в таких же скрубберах и под таким же давлением, как и очистка от СО. [7]
При изменении парциального давления окиси углерода в указанных пределах она не имеет тенденции ни к увеличению, ни к уменьшению. [8]
Так, уменьшение парциального давления окиси углерода в газе в период разработки значительно повышает его активность, увеличивает выходы жидких продуктов и содержание в них парафиновых фракций. [9]
Кроме равновесия между парциальным давлением окиси углерода в газе и концентрацией комплексного соединения одновалентной меди и окиси углерода, устанавливается также равновесие ( в растворе) между одновалентной медью и СО2, с одной стороны, и двухвалентной медью и абсорбированной СО, с другой. [10]
Каким же должно быть парциальное давление окиси углерода в газах восстановительной печи, чтобы реакция восстановления могла начаться с температуры 1300 К. При заданной температуре реакция, очевидно, сможет получить развитие при условии, что фактическое давление окиси углерода будет ниже равновесного. [11]
При повышении концентрации или парциального давления окиси углерода равновесие смещается вправо. Значительная часть гемоглобина оказывается превращенной в карбоксигемоглобин и перестает участвовать в переносе кислорода к тканям. [12]
Выше этого предела изменение парциального давления окиси углерода не приводит к изменению изомерного состава продуктов реакции гидроформилирования и скорости изомеризации олефина в ходе реакции гидроформилирования. Кроме того, выше этого предела стираются различия между комплексными соединениями родия как катализаторами реакции гидроформилирования - в этой области парциального давления окиси углерода изомерный состав продуктов реакции одинаков для всех исследованных нами соединений родия. Это позволяет предположить, что различные комплексные соединения родия в данной области парциального давления окиси углерода превращаются в одно каталитически активное соединение - карбо-нил родия. [13]
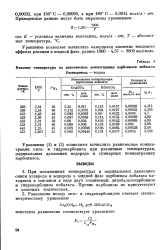 |
Влияние температуры на равновесные концентрации карбонилов кобальта. [14] |
При повышенных температурах и парциальных давлениях окиси углерода и водорода в жидкой фазе карбонилы кобальта находятся в основном в виде двух соединений: дикобальтокарбонила и гидрокарбонила кобальта. Прочие карбонилы не присутствуют в заметных количествах. [15]
Страницы: 1 2 3 4