Парциальное давление - окись - углерод
Cтраница 2
Так, неэффективными оказались увеличение парциального давления окиси углерода, работа при возможно более низкой температуре, добавление сероуглерода для подавления гидрирования, использование параформаль-дегида вместо СО Н2 и применение в качестве растворителя метанола. Были испытаны вместо СО Н2 смеси СО с водой, СО со спиртом в надежде получить хороший выход диметилпробковой кислоты или ее эфира. [16]
При повышении температуры и снижении парциального давления окиси углерода увеличивается роль механизма, предлагаемого Рудковским, Пажитновым и Джонсоном. [17]
Скорость восстановления зависит главным образом от парциального давления окиси углерода, а не от давления водорода. [18]
Это равновесие хорошо объясняет тормозящее влияние парциального давления окиси углерода на скорость карбонилирования. [19]
В работе показано, что влияние парциального давления окиси углерода и температуры на изомерный состав продуктов гидрофор-милирования удовлетворительно объясняется их более сильным влиянием на стадию разложения ацилкобальткарбонилов, чем на изомеризацию последних. [20]
Скорость разложения зависит от температуры и парциального давления окиси углерода. [21]
Направлен кг реакции определяется температурой и парциальным давлением окиси углерода: при высоких парциальных давлениях СО происходит образование карбоннлов кобальта, при низких - их разложение, 11рн исследовании равновесия в системе металлический кобальт - карбопилы установлено, что с повышением температуры для сохранения карбошлон необходимо упелнчивать давление окиси углерода. [22]
Установлена идентичность зависимости скоростей реакций от соотношения парциальных давлений окиси углерода и водорода для реакций гидроформилирования и перехода солей кобальта в карбонилы и дано объяснение этому явлению. [23]
В настоящем сообщении приведены результаты исследования влияния парциального давления окиси углерода, циркуляции газа и скорости подачи растворителя на полноту образования карбонилов ( кобальтизации), а также условий образования кар-бонилов из порошка кобальта, полученного в процессе термической декобальтизации без носителя. [24]
Это уравнение дает связь между равновесными значениями парциального давления окиси углерода и температуры. Задавшись температурой, мы находим равновесное ей значение парциального давления и, наоборот, по заданному ( нестандартному) давлению можем определить температуру термодинамического равновесия в нестандартных условиях. [25]
Установлена идентичность зависимости скоростей реакций от соотношения парциальных давлений окиси углерода и водорода для реакций гидроформилирования и перехода солей кобальта в карбонилы и дано объяснение этому явлению. [26]
 |
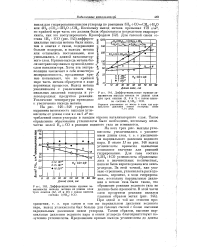
Скорости гидрокарбовшлнро-вания циклогексена в зависимости от давлений СО и Н2. Опыты постоянной продолжительности. давле. [27] |
Очевидно, таким образом, что повышение парциального давления окиси углерода сверх некоторой оптимальной величины значительно уменьшает скорость реакции. При неизменном давлении окиси углерода увеличение скорости, приблизительно пропорционально возрастанию давления водорода. [28]
Экспериментально установлена зависимость между температурой реакции и парциальным давлением окиси углерода, необходимым для обеспечения устойчивости карбонилов кобальта в реакторе. [29]
Страницы: 1 2 3 4