Дж-моль
Cтраница 4
Эти простые эффекты сближения находят свое отражение в энтропии активации реакции. Величины энтропии активации эффективных внутримолекулярных реакций примерно на 80 Дж-моль 1 - Кг1 более положительны, чем те же параметры соответствующих межмолекулярных процессов, так как включение реагирующих групп в одну и ту же молекулу понижает молекулярность реакции до единицы. Энтальпии активации, с другой стороны, в этих случаях не обязательно сильно различаются. Известно много примеров, когда последние параметры для внутри - и межмолекулярных реакций совпадают в пределах ошибки эксперимента. [46]
В свою очередь значения ДСр вычислены либо как р - Ср, либо из темг пературыой зависимости энтальпий растворения. Наиболее типичные значения погрешностей лежат в пределах 3 - 6 Дж-моль - К - - Значения, стоящие в скобках, относятся к концентрациям порядка 0 3 % ( мол. [47]
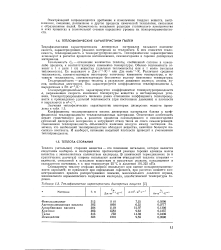 |
Теплофизические характеристики дисперсных веществ. [48] |
Ее выражают в Дж - г - - К 1 или Дж-моль - К. Различают среднюю теплоемкость, соответствующую некоторому конечному изменению температуры, и истинную теплоемкость, соответствующую бесконечно малому изменению температуры. [49]
 |
Значения С 2 при 298 К для неэлектролитов Н ( СН2 ПХ в водном растворе. [50] |
Это позволило авторам [128] предположить, что вклад группы Н-X в С 2 одинаков и не зависит от того, соединены ли Н и X непосредственно или через какое-то число СН2 - групп. Для вклада метиленовой группы при 298 К было принято значение бссн2 90 Дж-моль - - К -, использование которого позволило определить данные для других групп. [51]
Вращательное сверхравновесное возбуждение частиц не может повлиять на ход химической реакции. Потеря вращательного возбуждения происходит за несколько соударений, а квант вращательной энергии ( - 102 Дж-моль -) не может привести к заметному изменению реакционной способности частиц. [52]
Дж-моль - К 1; Тпя-температура плавления, К. Так, для золота ( Гпл1336 К) вычисленная по формуле (6.129) энергия активации составляет 2 - Ю5 Дж-моль 1, что достаточно хорошо совпадает со значением Ql9-105 Дж-моль - 1, полученным из экспериментов с применением метода меченых атомов. [53]
 |
Температурная зависимость орто - пара состава водорода.| Точки кипения и тройные точки нормального и равновесного водорода. [54] |
Неравновесные смеси орто - и параводорода имеют температуры тройных точек и точек кипения в промежутках между значениями, указанными в табл. 4.3. В связи с этим состав водорода, использующегося для реализации температуры репернойс точки, должен быть определен. Поскольку орто-пара конверсия направлена к состоянию с более низкой энергией, переход, от высокотемпературного к низкотемпературному равновесному состоянию сопровождается выделением тепла, составляющим около 1300 Дж-моль 1 при 20 К. Выделяющееся при конверсии тепло приводит к тому, что водород, залитый в сосуд Дью-ара сразу после ожижения, испаряется при хранении более чем: наполовину. [55]
Дж-моль - К 1; Тпя-температура плавления, К. Так, для золота ( Гпл1336 К) вычисленная по формуле (6.129) энергия активации составляет 2 - Ю5 Дж-моль 1, что достаточно хорошо совпадает со значением Ql9-105 Дж-моль - 1, полученным из экспериментов с применением метода меченых атомов. [56]
Страницы: 1 2 3 4