Двуокись - церие
Cтраница 1
Двуокись церия в серной кислоте при 90 оказывается достаточно энергичным окислителем для получения альдегида окислением метильной группы. [1]
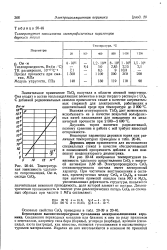 |
Температурная зависимость удельного сопротивления, Ом - м, оксида. [2] |
Двуокись церия применяется для изготовления специальных стекол в качестве обесцвечивающей и повышающей прозрачность добавки и как компонент конденсаторного диэлектрика. [3]
Двуокись церия в сернокислом растворе также является сильным окислителем. Толуол окисляется при 60 - 90 двуокисью церия в 60 % - ной серной кислоте в бензальдегид; под конец реакции масса от образовавшегося сернокислого церия превращается в белую кашицу. [4]
Двуокись церия растворяется в концентрированной азотной кислоте при нагревании до кипения. Для восстановления церия до трехвалентного в раствор периодически добавляется перекись водорода. [5]
Двуокись церия СеО2 - белый с желтоватым оттенком плотный кристаллический порошок. Разница в оттенках зависит от размера зерен окиси. Различные оттенки окраски могут быть объяснены также наличием примесей окислов других РЗЭ. Высокая теплота образования обусловливает значительную ее устойчивость. Растворимость улучшается в присутствии восстановителя. До полуторной окиси восстанавливается кальцием. Растворяется полностью в серной кислоте при температуре ее кипения; в присутствии гидрохинона растворение протекает при более низкой температуре. [6]
Двуокись церия в серной кислоте при 90 оказывается достаточно энергичный окислителем для получения альдегида из метилового замещенного. [7]
Двуокись церия получается при прокаливании оксалата, карбоната или других солей церия ( III) при доступе воздуха. С, фильтруют и определяют титр этого раствора при помощи раствора соли Мора. [8]
Двуокись церия применяется для обесцвечивания стекла. Стекла, содержащие двуокись церия, не теряют прозрачности при облучении солнцем и под действием радиации. Двуокись церия применяется для изготовления защитных прозрачных стеклянных блоков в ядерной технике. [9]
Двуокись церия оказалась хорошим катализатором в процессе гидрогенизации СО; она же способствует быстрому протеканию реакции дегидрогенизации спиртов. Окись празеодима Рг203 катализирует окисление аммиака при низких температурах. Такие процессы, как электрохимическое окисление анилина в хинон или превращение S0a в S03, в большой степени ускоряются в присутствии ионов церия. [10]
Двуокись церия упаковывают в стеклянные банки с пластмассовой крышкой. [11]
Двуокись церия не растворима в воде, кислотах ( кроме горячей концентрированной H2SO4), щелочах, перекисях щелочных металлов. При сплавлении с полуторными окислами редкоземельных металлов СеО2 образует твердые растворы. [12]
Двуокись церия получается, главным образом, из монацитовых песков. Ее применяют в качестве глушителя только в виде добавки при размоле эмали. Двуокись церия не ядовита. Считают, что в качестве глушителя она действует1 в два раза сильнее, чем окись олова, и в три раза сильнее, чем окись сурьмы. Глушащей способности окиси церия сильно помогает повышенное содержание в эмали глинозема, окислов кальция и магния и двуокиси циркония. [13]
Двуокись церия в серной кислоте при 90 оказывается достаточно энергичным окислителем для получения альдегида окислением метальной группы. [14]
Двуокись церия Се02 с температурой плавления около 2600 - 2800 С характеризуется отсутствием полиморфных превращений и устойчивостью при нагревании в окислительной среде; в восстановительной среде она переходит в менее огнеупорную форму Се203 ( - 1700е С) и дает карбид ( СеС2) при 1600 С. Изделия из Се02 могут быть изготовлены обычными методами. Температура, необходимая для обжига, около 1600е С. Повышенный коэффициент термического расширения ( около 13 10 - 6 при 1000 С) обусловливает снижение термической стойкости. Сведений об областях применения керамики из двуокиси церия нет, очевидно, в связи с малым ее использованием из-за большой склонности к восстановлению. [15]
Страницы: 1 2 3 4