Двуокись - церие
Cтраница 2
Двуокись церия применяется для обесцвечивания стекла. Стекла, содержащие двуокись церия, не теряют прозрачности при облучении солнцем и под действием радиации. Двуокись церия применяется для изготовления защитных прозрачных стеклянных блоков в ядерной технике. [16]
Двуокись церия СеО2 - белый с желтоватым оттенком плотный кристаллический порошок. Разница в оттенках зависит от размера зерен окиси. Различные оттенки окраски могут быть объяснены также наличием примесей окислов других РЗЭ. Высокая теплота образования обусловливает значительную ее устойчивость. Растворимость улучшается в присутствии восстановителя. До полуторной окиси восстанавливается кальцием. Растворяется полностью в серной кислоте при температуре ее кипения; в присутствии гидрохинона растворение протекает при более низкой температуре. [17]
Двуокись церия - порошковидный продукт, применяется в лабораторной практике и для различных технических целей. [18]
Двуокись церия Се02 с температурой плавления около 2600 - 2800 С характеризуется отсутствием полиморфных превращений и устойчивостью при нагревании в окислительной среде; в восстановительной среде она переходит в менее огнеупорную форму Ce20s ( - 1700е С) и дает карбид ( СеС2) при 1600 С. Изделия из Се02 могут быть изготовлены обычными методами. Температура, необходимая для обжига, около 1600е С. Повышенный коэффициент термического расширения ( около 13 10 - 6 при 1000 С) обусловливает снижение термической стойкости. Сведений об областях применения керамики из двуокиси церия нет, очевидно, в связи с малым ее использованием из-за большой склонности к восстановлению. [19]
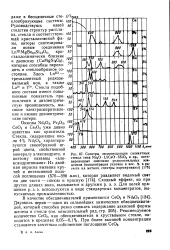 |
Спектры люминесценции силикатных стекол типа NasO 1 5СаО 5SiO2 и др., активированных окислами редкоземельных элементов ( концентрация указана в вес. % в расчете на металл, спектры нормированы. [20] |
N Двуокись церия - один из сильнейших химических обесцвечивателей, который способен резко снижать содержание закисной формы железа в стекле ( см. окислительный ряд, стр. [21]
Помимо двуокиси церия ( не менее 45 %) и окислов других редкоземельных элементов ( более 48 %) содержит двуокись тория ( следы), окись натрия ( свыше 0 1 %), двуокись кремния ( - 1 %), небольшие к-ва пятиокиси фосфора и окислов железа. [22]
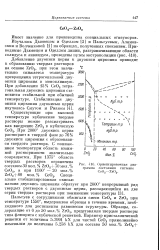 |
Ориентировочная диаграмма состояния системы Се02 - Zr02. [23] |
Добавление двуокиси церия к двуокиси циркония приводит к образованию твердых растворов на основе Zr02, при этом значительно снижается температура превращения тетрагональной двуокиси циркония в моноклинную. При добавлении 15 % Се02 тетрагональная двуокись циркония становится стабильной при обычной QQQ температуре. [24]
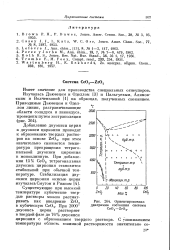 |
Ориентировочная диаграмма состояния системы. [25] |
Добавление двуокиси церия двуокиси циркония приводит к образованию твердых растворов на основе Zr02, при этом - значительно снижается температура превращения тетрагональной двуокиси циркония в моноклинную. При добавлении 15 % Се02 тетрагональная двуокись циркония становится стабильной при обычной температуре. [26]
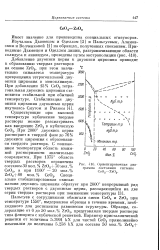 |
Ориентировочная диаграмма состояния системы Се02 - Zr02. [27] |
При 2000 двуокись церия растворяет в твердой фазе до 76 % 50 - двуокиси циркония с образованием твердого раствора. С понижением температуры область взаимной растворимости значительно сокращается. [28]
Теплота образования двуокиси церия из элементов составляет 223 4 ккал / моль. [29]
Найдено, что двуокись церия с ортоуранатом кальция образует простую эвтектику, которая плавится при 1760 С; заметной взаимной растворимости компонентов при этой температуре не наблюдается. В ортоуранате стронция СеО2 растворяется. Взаимодействие двуокиси церия с Ва31Ю6 интересно тем, что образующийся твердый раствор является раствором СеО2 в р-модификации ортоураната. Растворимость СеО2 в р - Ва31Ю6 составляет около 25 % при 1200 С. [30]
Страницы: 1 2 3 4