Дегидратация - третичный спирт
Cтраница 2
При получении этилена в качестве дегидратирующего средства может быть использована метафосфорная кислота. Дегидратация третичных спиртов происходит при кипячении их с безводной щавелевой кислотой или бисульфатом калия. Все третичные спирты и некоторые вторичные легко дегидратируются при перегонке в присутствии иода, взятого в количестве пример но 0 2 % от веса спирта. Таким образом, наиболее легко подвергаются дегидратации третичные спирты, затем вторичные и труднее всего превращаются в олефины первичные спирты. [16]
При получении этилена в качестве дегидратирующего средства может быть использована метафосфорная кислота. Дегидратация третичных спиртов происходит при кипячении их с безводной щавелевой кислотой или бисульфатом калия. Все третичные спирты и некоторые вторичные легко дегидратируются при перегонке в присутствии иода, взятого в количестве примерно 0 2 % от веса спирта. Таким образом, наиболее легко подвергаются дегидратации третичные спирты, затем вторичные и труднее всего превращаются в олефи-ны. [17]
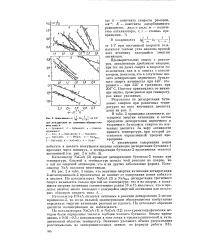 |
Зависимость Is - In - - - - - от 1 / 1. [18] |
Из рис. 2 и табл. 3 видно, что величина энергии активации дегидратации 2-метилпропанола - 2 практически не зависит от содержания ионов кобальта в цеолите. На катализаторах NaCoA ( 2) и NaAHOX дегидратация третичного спирта начинается только при той же температуре, что и на кварце, а кажущиеся энергии активации соответственно равны 16 и 15 ккал / молъ, что в пределах ошибок опыта совпадает с кажущейся энергией активации для остальных образцов цеолита типа А. [19]
Арбузов и И. А. Арбузова [33] подробно исследовали взаимодействие бензофенона с бромистым и йодистым циклогексилмагнием. В первом случае были выделены бензгидрол, бензопинакон и продукт дегидратации третичного спирта - циклогексилидендифенилметан. Во втором случае получены, кроме неизмененного бензофенона, бензопинакон, дициклогек-сил, немного дифенилциклогексилкарбинола, циклогексилидендифенилметан, тетрафенилэтан. С точки зрения изложенной выше радикальной схемы затруднительно только объяснение образования тетрафенилэтилена. По Дэвису [40], результаты реакции бензофенона с бромистыми н-амил, изо-амил и р-метилбутилмагнием также согласуются с этой схемой. [20]
Нодакенетин ( LIII), [ аЬ - 22 4, содержится в виде глюкозида, нода-кенина СаоНаэОд - НаО, в Peucedanum decursivum Maxim. Перегонка нодакенетина с пятиокисью фосфора в высоком вакууме дает ангидронода-кенетин, образующийся при дегидратации третичного спирта, строение которого может быть выражено формулой LIV или, более вероятно, LIVa. Гидрирование соединений LIV приводит к тетрагидронодакенетину, идентичному дезоксидигидроореоселону ( LV) ( стр. При окислении щелочным раствором перманганата калия из изопропилиденовой группы фуранового кольца образуется ацетон. [21]
Ниже приведены спектральные линии исследованных углеводородов. Все 1-метил - 2-алкилциклогексаны были получены по Гриньяру взаимодействием алкилмагнийбромидов с 2-метилциклогексаноном, дегидратацией полученного третичного спирта, гидрированием непредельного углеводорода и разгонкой стереоизомеров на колонке 100 т.т. 1 4 - Диизопропилциклогек-саны были получены гидрированием 1 4-диизопропилбензола и разгонкой на стереоизомеры на такой же колонке. На всех стадиях синтезов принимались меры для получения исходных, промежуточных и конечных веществ в возможно более чистом виде. Все перечисленные углеводороды, кроме 1-метил - 2-этилциклогексанов, получены впервые. [22]
Образовавшийся смешанный алкоголят магния после нагревания реакционной смеси разлагают подкисленной водой. При синтезе третичных спиртов для разложения используют водный раствор хлористого аммония, так как в присутствии минеральных кислот может происходить дегидратация третичного спирта. [23]
Рекомендуется также вести разложение при низкой температуре. Перегонку продукта в тех случаях, когда температура кипения его достаточно высока, следует проводить при пониженном давлении, иначе возможна дегидратация третичного спирта в процессе перегонки. Следы иода катализируют реакцию дегидратации, поэтому при синтезе легко дегидратирующихся спиртов активацию магния иодом не проводят. [24]
Чтобы избежать дегидратации, при получении третичных спиртов разложение следует производить насыщенным водным раствором хлористого аммония, а не разбавленными кислотами ( ионы водорода каталитически ускоряют дегидратацию), при низкой температуре. Перегонку продукта в тех случаях, когда температура кипения его достаточно высока, следует проводить при пониженном давлении, иначе возможна дегидратация третичного спирта в процессе перегонки леды иода катализируют реакцию дегидратации, поэтому при синтезе легко дегидратирующихся спиртов активацию магния иодом не проводят. [25]
Чтобы избежать дегидратации, при получении третичных спиртов разложение следует производить насыщенным водным раствором хлористого аммония, а не разбавленными кислотами ( ионы водорода каталитически ускоряют дегидратацию), при низкой температуре. Перегонку продукта в тех случаях, когда температура кипения его достаточно высока, следует проводить при пониженном давлении, иначе возможна дегидратация третичного спирта в процессе перегонки Следы иода катализируют реакцию дегидратации, поэтому при синтезе легко дегидратирующихся спиртов активацию магния иодом не проводят. [26]
Реакции ( прямая и обратная) катализируются кислотами и основаниями; в основных растворах при высоких концентрациях реагирующих веществ они осложняются образованием полимеров с общей формулой Н - fCH2 - C ( R) ( OH) ] n - ОН. В зависимости от природы R образующийся в результате реакции диол может превращаться в альдегид или кетон. В кислых растворах дегидратация третичного спирта приводит к образованию а р-ненасыщенных кетонов [ например, R - С ( СН3) СН - CO ( R) ], которые могут подвергаться дальнейшей конденсации. [27]
Реакции ( прямая и обратная) катализируются кислотами и основаниями; в основных растворах при высоких концентрациях реагирующих веществ они осложняются образованием полимеров с общей формулой Н - [ СН2 - C ( R) ( OH) ] n - ОН. В зависимости от природы R образующийся в результате реакции диол может превращаться в альдегид или кетон. В кислых растворах дегидратация третичного спирта приводит к образованию а, Р - ненасыщенных кетонов [ например, R - С ( СН3) СН - CO ( R) ], которые могут подвергаться дальнейшей конденсации. [28]
Изобутилен удаляется из реакционной смеси путем отгонки, и при соответствующем подборе условий реакции он легко может стать основным продуктом. Если изобутилен не удаляется по мере его образования, то основным конечным продуктом является полимер. Серная кислота часто оказывается слишком энергичным агентом для дегидратации третичных спиртов; с целью получения лучших результатов используют бисульфат калия, сульфат меди, иод, фосфорную кислоту или пятиокись фосфора; эти агенты в меньшей степени вызывают полимеризацию и окислительную деструкцию, которая в случае серной кислоты приводит к образованию сернистого газа. [29]
Дегидратация спиртов является в основном кислотнокатализи-руемой реакцией. Тафтом с сотрудниками [75-77] была проведена большая работа по выяснению ее механизма. Эти исследования показали, что промежуточное соединение при дегидратации третичных спиртов или при гидратации разветвленных олефинов в разбавленных растворах кислот напоминает сопряженную оле-финовую кислоту, которая более или менее свободна от ковалентно связанной воды. Это фактически является определением иона кар-бония, и его существование в реакции третичных спиртов считают достаточно хорошо доказанным. [30]
Страницы: 1 2 3