Дегидрогенизация - бутилен
Cтраница 3
На заводах производства бутадиена двухступенчатым дегидрированием природных газов фракция С4 свободна от олефинов. Во второй ступени производится дегидрогенизация бутиленов, полученных при дегидрогенизации к-бутана. Бутилены должны предварительно подвергаться фракционированному разделению под давлением и экстрактивной перегонке с ацетоном или фурфуролом. [31]
В 1957 г. Баландин, Нейман, Богданова, Исагулянц, Щеглова и Попов [193, 194] дегидрировали смеси бутана и бутилена, содержащие в молекуле одного из компонентов радиоактивный атом углерода. В результате было установлено, что образование дивинила происходит практически только за счет дегидрогенизации бутилена; бутан же непосредственно в дивинил практически не превращается. [32]
Так, для реакций, в энергетическом балансе которых фигурирует энергия сопряжения, можно брать катализаторы с меньшим адсорбционным потенциалом. Например, для дегидрогенизации циклогексана оказались пригодна окись кадмия, но не пригодна окись цинка, а для дегидрогенизации бутилена пригодна не только окись кадмия, но и окись цинка, тогда как окислы щелочноземельных металлов непригодны. Перечисленные зависимости уже сейчас позволяют предвидеть каталитическое действие для некоторых однотипных реакций и должны быть учтены в дальнейшем при решении проблемы подбора катализаторов. [33]
То, что для реакций, при которых выделяется энергия сопряжения, можно брать катализаторы с меньшим адсорбционным потенциалом, тоже оправдалось на опыте. Так, например, для дегидрогенизации циклогексана пригоден тот же кадмий, но непригоден цинк, а для дегидрогенизации бутилена пригодна не только окись кадмия, но и окись цинка, тогда как окиси щелочноземельных металлов непригодны. [34]
То, что для реакций, в энергетическом балансе которых фигурирует энергия сопряжения, можно брать катализаторы с меньшим адсорбционным потенциалом, тоже оправдалось на опыте. Так, например, для дегидрогенизации циклогексана оказался пригоден тот же кадмий, но непригоден цинк, а для дегидрогенизации бутилена пригодна не только окись жадмия, но и окись цинка, тогда как окиси щелочноземельных металлов непригодны. [35]
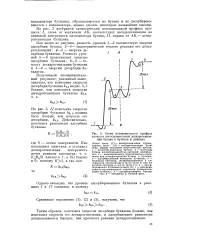 |
Схема потенциального профиля процесса последовательной дегидрогенизации бутана в бутилен и дивинил. [36] |
Цифры указывают энергетические уровни: 1 - исходной молекулы бутана; 2 - молекулы бутана, адсорбированной на активной поверхности; з - активированного мультиплетного комплекса при дегидрогенизации бутана в бутилен; 4 - адсорбированной молекулы бутилена; 5 - молекулы бутилена, дссорбировавшейся с поверхности катализатора в газ ( в части I) или же энергии бутилена в газе ( в части II); 6 - адсорбированного бутилена ( в части II); 7 - активированного мультиплетного комплекса дегидрогенизации бутилена; - адсорбированного бутадиена; 9 - бутадиена в газовой фазе. [37]
Для производства из бутиленов бутадиена в США применяется процесс Джерси. Сырье, содержащее около 70 % бутнленов, смешивается при 595 с 10 - 20 объемами пара при температуре 705 и проходит через слой катализатора. Дегидрогенизация бутиленов проводится при температуре 620 - 680 и времени контакта 0 2 сек. Для предотвращения полимеризации бутадиена в системе при помощи водяного пара поддерживается низкое его парциальное давление. [38]
Для производства из бутиленов бутадиена в США применяется процесс Джерси. Сырье, содержащее около 70 % бутиленов, смешивается при 595 с 10 - 20 объемами пара при температуре 705 и проходит через слой катализатора. Дегидрогенизация бутиленов проводится при температуре 620 - 680 и времени контакта 0 2 сек. Для предотвращения полимеризации бутадиена в системе при помощи водяного пара поддерживается низкое его парциальное давление. [39]
Катализатор содержит 98 % фосфата никеля и кальция GaeNi ( Р04) б и 2 % окиси хрома. Характерным для этого катализатора является то, что он не вызывает побочных реакций. Он способствует протеканию реакций распада и дегидрогенизации бутиленов до ацетилена и реакций их окисления до ацетона. [40]
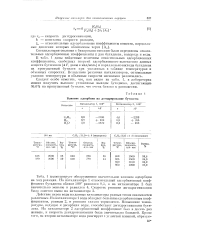 |
Влияние адсорбции на дегидрирование бутилена. [41] |
Действие паров воды на данные катализаторы разных типов оказывается различным. На катализаторе 1 вода обладает большим адсорбционным коэффициентом, равным 2, и реакция сильно тормозится. Повышение температуры, ведущее к десорбции воды, способствует дегидрогенизации бутилена. На катализаторе 2 адсорбционный коэффициент был в десять раз меньше, и скорость дегидрогенизации была значительно большей. [42]
Окись цинка многократно исследовалась как п-полупро-водник. На возможность объединенного подхода к ее каталитическим свойствам, с точек зрения электронной и мульти-плетной теорий, указали Доуден, Маккензи и Тепнел [373] ( ср. Автор и И. Д. Рождественская [374] определили для этого катализатора е для дегидрогенизации бутилена ( эти определения проведены совместно с О. К. Богдановой и А. П. Щегловой), изопропилового спирта и пиперидина. Отсюда были найдены адсорбционные потенциалы. Окись цинка не дегидрировала циклогексан и бутан, и это означает, что дегидрирование бутилена происходит вследствие появления энергии сопряжения в бутадиене, в согласии с тем, что было сказано выше ( гл. [43]
Применение метода дифференциальной термопары, разработанного В. В. Патрикеевым и автором [319, 320] при исследовании катализа спиртов окислами титана, иттрия и др. в работах А. А. Толстопятовой, автора и И. Р. Коненко [321-326], показало, что эти окислы, сначала оказывающие дегидрирующее действие, вскоре покрываются углистыми отложениями и проявляют дегидратирующее действие. Окись хрома и окись цинка не показывают такого эффекта. Последний необходимо учитывать при катализе окислами. Автор, О. К. Богданова и А. П. Щеглова [107] нашли, что хромовый катализатор дегидрогенизации бутилена долго не снижает своей активности, несмотря на образование угля. Поскольку на окислах образуются не дендриты, а смолистые пленки, то отсюда был сделан вывод, что молекулы продуктов разложения мигрируют по поверхности, освобождая активные центры и накапливаясь на неактивных участках. [44]
 |
Двойной лабораторный хроматограф. [45] |
Страницы: 1 2 3 4