Дегидрогенизация - спирт
Cтраница 2
Баландин совместно с Борком [257] изучили, кроме того, реакции дегидрогенизации спиртов на меди. Была определена зависимость продолжительности жизни молекул спиртов и образовавшихся на их основе альдегидов от температуры и истинной энергии активации дегидрогенизации алкоголей. [16]
Гноевый [2] открыл реакции этого типа, изучая вначале влияние освещения на дегидрогенизацию спиртов или муравьиной кислоты на поверхности окиси цинка. В усовершенствованном приборе, названном Вейсом [3] реактором Шваба, Гноевый освещал каталитический сосуд видимым или ультрафиолетовым светом длинноволновой области и изучал реакции в области температур от 250 до 450 с интервалами по 100 при повышении и понижении температуры. [17]
Катализаторы, состоящие из меди, смешанной с активаторами, и применяемые для дегидрогенизации спиртов в эфиры, можно регенерировать плавлением вместе с алюминием. Доказано, что после отделения алюминия катализатор приобретает даже более высокую активность, чем исходный материал. Например, катализатор, полученный из сплавленной меди или сплава меди с соответствующим каталитически активным веществом и потерявший активность, можно регенерировать, смешивая его с равным количеством алюминия в графитовом тигле при 600 - 800 и экстрагируя на водяной бане 10 % раствором едкого натра. [18]
Установил, что магний, кадмий, марганец, цинк и их окислы вызывают дегидрогенизацию спиртов, а алюминий, вольфрам, кремний и их окислы - дегидратацию. [19]
На этой стадии приготовления катализатор еще содержит избыток окиси меди и в таком состоянии пригоден для дегидрогенизации спиртов и гидрирования легко восстанавливающихся веществ, например нитросоединений. [20]
Двуокись церия оказалась хорошим катализатором в процессе гидрогенизации СО; она же способствует быстрому протеканию реакции дегидрогенизации спиртов. Окись празеодима Рг203 катализирует окисление аммиака при низких температурах. Такие процессы, как электрохимическое окисление анилина в хинон или превращение S0a в S03, в большой степени ускоряются в присутствии ионов церия. [21]
Действительно, расчет дал, что энергия активации дегидрогенизации предельного углеводорода EI ( вычисленная из энергий активации дегидрогенизации спирта ЕЗ и дегидратации последнего ЕЗ над катализаторами, осажденными едким натром из растворов сульфата) равна 97 8 для ВеО, 91 7 для MgO, 45 6 для ZnO и 35 4 ккал ( средн. Последняя из этих величин уже настолько мала, что дегидрогенизация предельного углеводорода становится возможной. [22]
Из рис. 1 видно, что для всех металлов, имеющих кубическую гра-нецентрированную решетку А1, величины энергии активации дегидрогенизации спирта изменяются параллельно с межатомным расстоянием металла. Зависимость величин энергии активации от межатомного расстояния металла передается прямой. [23]
Основными реакциями каталитического превращения изобутилово-го спирта в присутствии активированного медного катализатора при температурах 275 - 325 С являются реакции дегидрогенизации спирта до альдегида и реакция конденсации альдегида в сложный эфир - изобу-тилизобутират. При температурах 350 - 400 С выход сложного эфира падает и одновременно растет выход альдегида и кетона, что указывает на изменение функции катализатора. Имеющая место при низких температурах - ( 250 - 300 С) реакция сложноэфиряой конденсации сменяется новой реакцией превращения образовавшегося альдегида в соответствующий кетон. Значительное количество кетона получается лишь при температурах выше 400 С, когда в составе конденсата содержание альдегида и исходного спирта сильно снижается. [24]
Основными реакциями каталитического превращения изобутилово-го спирта в присутствии активированного медного катализатора при температурах 275 - 325 С являются реакции дегидрогенизации спирта до-альдегида и реакция конденсации альдегида в сложный эфир - изобу-тилизобутират. При температурах 350 - 400 С выход сложного эфира падает и одновременно растет выход альдегида и кетона, что указывает на изменение функции катализатора. Имеющая место при низких температурах ( 250 - 300 С) реакция сложноэф ирной конденсации сменяется новой реакцией превращения образовавшегося альдегида в соответствующий кетон. Значительное количество кетона получается лишь при температурах выше 400 С, когда в составе конденсата содержание альдегида и исходного спирта сильно снижается. [25]
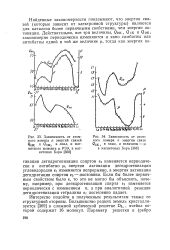 |
Зависимость от атомного номера л энергий связей.| Зависимость от атомного номера п энергии связи QCK ( в ккал, и величины - ц в магнетонах Бора. [26] |
Если бы более первичным свойством было е, то это не могло бы объяснить, почему, например, при дегидрогенизации спирта е2 изменяется периодически с изменением п, а при аналогичной реакции дегидрогенизации тетралина ei постепенно падает. [27]
Оказалось, что эти полимеры имеют весьма интересные электрические и магнитные свойства и обладают каталитической активностью в реакции окисления и дегидрогенизации спиртов. [28]
Свои последующие работы Платонов с сотрудниками [29-37] вели в двух направлениях: 1) применение рения и его соединений в качестве катализаторов при дегидрогенизации спиртов с получением альдегидов и кетонов; 2) при каталитическом окислении органических веществ. [29]
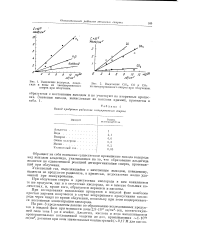 |
Выделение водорода, альдегида и воды из эвакуированного спирта при облучении. [30] |
Страницы: 1 2 3 4