Дегидроксилирование
Cтраница 2
В случае дегидроксилирования при повышенных температурах образцов кремнезема, содержащих примеси, адсорбционные и хемосорбционные свойства поверхности становятся еще более сложными. В работах [28, 29, 52, 53] исследовались теплоты адсорбции молекул, способных к сильному специфическому взаимодействию, например триэтиламина ( см. рис. 20 и 21) и тетра-гидрофурана, при увеличении степени дегидроксилирования поверхности аэросилогеля, содержавшего около 0 36 вес. [16]
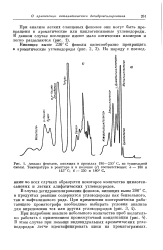 |
Анализ фенолов, кипящих в пределах 180 - 230 С, из туннельной смолы. Температура в реакторе и в колонне ( 1 соответственно. а - 180 и. [17] |
В случае дегидроксилирования фенолов, кипящих выше 260 С, в продуктах реакции содержатся углеводороды как бензольного, так и нафталинового ряда. [18]
Без обработки для дегидроксилирования можно использовать катализатор, предназначенный для ароматизации нафтенов способом ДНД. Катализатор приготовляется из окиси алюминия и сульфида алюминия и содержит около 15 % окиси молибдена. [19]
Среди стереоселективных методов дегидроксилирования наиболее известным является метод Кори - Винтера, основанный на смм-элиминировании из циклических производных. [20]
С ростом температуры дегидроксилирования ионообменная емкость по NH - иону падает приблизительно на 50 % по сравнению с исходной величиной. Кривая имеет перегиб, указывающий на образование промежуточных соединений при прокаливании. [21]
Среди стереоселективных методов дегидроксилирования наиболее известным является метод Кори - Винтера, основанный на сии-элиминировании из циклических производных. [22]
В заданных условиях дегидроксилирования при 200 образуются только циклогексановые, а при 350 - почти полностью ароматические углеводороды. При температуре 320 из чистого бензола циклогексан не образуется, а при дегид-роксилировании оксибензола при той же температуре образуется значительное количество циклогексана. [23]
Для изучения механизма дегидроксилирования и дегидратации Киселевым, Лыгиным и Галкиным использовано различие в принадлежности полос 4580 и 5290 см-1 структурным гидро-ксильным группам и адсорбированным молекулам воды. Как следует из рис. 45, после откачки образца пористого стекла при 100 к 200 С ( кривые 3 и 4) интенсивность полосы поглощения 4580 см-1 увеличивается, полоса же поглощения 5290 см-1 практически исчезает. Наблюдаемое после откачки при 300 С дальнейшее уменьшение интенсивности полосы поглощения 4580 см - свидетельствует о заметном дегидроксилировании поверхности. При этом изменение интенсивности полосы поглощения 5290 см-1 указывает на завершение дегидратации пористого стекла при температуре откачки около 200 С. [24]
С, обусловлен дегидроксилированием Са ( ОН) 2, находящейся в очень высокодиспе рсном состоянии, которая диссоциирует при несколько более низкой температуре, чем крупнокристаллический гидроксид кальция. Электронно-микро-скфшческий анализ указывает на наличие в микроструктуре портландцементного камня портландита в виде как крупноблочных кристаллов Са ( ОН) 2, так и тончайших пластин, сформированных в порах с включением кристалликов эттрингита. Причем содержание кальцита в этих же образцах, как показывает ДТА - минимально. На основании этого можно сделать вывод, что В / Ц 0 6; 0 7; 0 8 наиболее благоприятно сказывается на формировании портландцементного камня. [25]
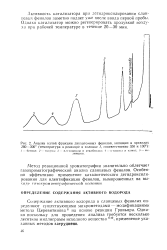 |
Анализ одной фракции двухатомных фенолов, кипящих в пределах 260 - 300 ( температура в реакторе и колонке /, соответственно 350 и 130. [26] |
Активность катализатора при дегидроксилировании сланцевых фенолов заметно падает уже после ввода первой пробы. Однако катализатор можно регенерировать продувкой воздуха при рабочей температуре в течение 20 - 30 мин. [27]
Я полагаю, что дегидроксилирование, как показано в случае редкоземельных форм цеолитов, помимо среднего расстояния между гидроксильными группами зависит от многих факторов. [28]
В случае протекания реакции дегидроксилирования по схеме (IV.1) происходит смыкание соседних гидроксильных групп поверхности частиц кремнезема с образованием силоксановых мостиков, а при реакции по схеме (IV.2) происходит смыкание гидроксильных групп соседних частиц кремнеземов. Реакция по схеме (IV.1) происходит преимущественно при более низких температурах прокаливания. В работе [54] предполагается, что в такую реакцию прежде всего вступают те гидроксильные группы, которые связаны парами с поверхностными атомами кремния. В результате этого на поверхности кремнезема, обработанного при температуре выше 600 С, остаются гидроксильные группы, связанные преимуществено с одним атомом кремния. Однако, как уже рассматривалось, работы последнего времени по исследованию реакций поверхностных гидроксильных групп с хлор-производными различной структуры ( например, с молекулами SiCU и А1С13) указывают на большую концентрацию пар гидроксильных групп, связанных с одним атомом Si на поверхности, даже при высоких температурах дегидроксилирования. [29]
Большую роль в процессах дегидроксилирования и спекания играет время прокаливания. На этом основании сделано заключение о том, что механизм спекания за счет вязкого течения осуществляется легче процесса поверхностной диффузии. Наблюдаемое же снижение температуры спекания при добавлении примеси является следствием ускорения процесса вязкого течения. [30]
Страницы: 1 2 3 4