Дегидроксилирование - поверхность
Cтраница 4
Сидорова, центрами физической адсорбции молекул воды. Сидоров полагал, что интенсивность полосы при 3665 см 1 не должна меняться в процессе дегидроксилирования поверхности вследствие постоянства концентрации поверхностных центров второго рода, способных адсорбировать молекулы воды. [46]
 |
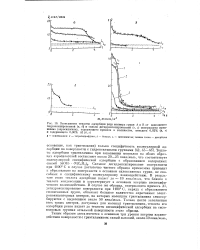
Зависимость энергии активации десорбции аммиака от его концентрации. [47] |
Увеличение парциального давления водорода, по мнению авторов, приводит к сдвигу равновесия реакции ( 1) влево, поэтому скорость процесса снижается. Падение активности цеолита при дальнейшем увеличении парциального давления водорода связано, по нашему мнению, с дегидроксилированием поверхности и уменьшением кислотности катализатора. [48]
В случае дегидроксилирования при повышенных температурах образцов кремнезема, содержащих примеси, адсорбционные и хемосорбционные свойства поверхности становятся еще более сложными. В работах [28, 29, 52, 53] исследовались теплоты адсорбции молекул, способных к сильному специфическому взаимодействию, например триэтиламина ( см. рис. 20 и 21) и тетра-гидрофурана, при увеличении степени дегидроксилирования поверхности аэросилогеля, содержавшего около 0 36 вес. [49]
Наличие на поверхности кремнезема таких примесей, как А1 и В, образующих сильные протонные и апротонные кислотные центры, вызывает увеличение энергии связи с электроподонорными молекулами. Это особенно сильно проявляется при дегидратации и дегидроксилировании поверхности, поскольку при этом обнажаются сильные апротонные кислотные центры. Дегидроксилирование поверхностей чистых кремнеземов снижает специфичность молекулярной адсорбции, уменьшая возможность образования водородной связи. Дегидроксилирование же кремнеземов, содержащих примеси А1 и В, приводит к сильному росту теплоты адсорбции молекул групп В и D. Этот эффект ярко проявляется на содержащих примеси А1 аэросилогелях после дегидроксилирования их поверхности при высоких температурах. Рост теплоты адсорбции связан с изменением именно химии поверхности, поскольку макропористые кремнеземы при этом практически не изменяют величину своей удельной поверхности и размеры пор и теплоты адсорбции молекул группы А не изменяются. [50]
Наличие на поверхности кремнезема таких примесей, как А1 и В, образующих сильные протонные и апротопные кислотные центры, вызывает увеличение энергии связи с электронодонорньтми молекулами. Это особенно сильно проявляется при дегидратации и дегидроксилировании поверхности, поскольку при этом обнажаются сильные апротонные кислотные центры. Дегидроксилирование поверхностей чистых кремнеземов снижает специфичность молекулярной адсорбции, уменьшая возможность образования водородной связи. Дегидроксилирование же кремнеземов, содержащих примеси А1 и В, приводит к сильному росту теплоты адсорбции молекул групп В и D. Этот эффект ярко проявляется на содержащих примеси А1 аэросилогелях после дегидроксилирования их поверхности при высоких температурах. Рост теплоты адсорбции связан с изменением именно химии поверхности, поскольку макропористые кремнеземы при этом практически не изменяют величину своей удельной поверхности и размеры пор и теплоты адсорбции молекул группы А не изменяются. [51]
Дегидратация чистых и достаточно крупнопористых кремнеземов с гидроксилированной поверхностью проходит практически полностью уже при комнатной температуре. На это указывают изменения в инфракрасных спектрах при адсорбции и десорбции пара воды как в области составных ( деформационного и валентного) [61], так и в области деформационных колебаний молекулы - воды. При более высоких температурах происходит лостепенное дегидроксилирование поверхности кремнезема, которое особенно интенсивно в области от 300 до 600 С. [52]
Сильное дегидроксилирование поверхности при 1100 С в случае достаточно чистого образца кремнезема приводит к образованию на поверхности в основном силоксановых групп, не способных к специфическому молекулярному взаимодействию. В результате этого теплота адсорбции падает до - 10 ккал / молъ, что близко к теплоте конденсации и характеризует в основном энергию неспецифического взаимодействия. В случае же образца, содержащего примесь А1, дегидроксилирование поверхности при 1100 С, наряду с образованием силоксановых групп, обнажает большое количество апротонных элект-роноакцепторных центров, на которых молекулы триэтиламина хемосор-бируются с выделением около 50 ккал / молъ. Только после заполнения всех таких центров, доступных для молекул триэтиламина, теплота его адсорбции резко падает до теплоты неспецифической адсорбции на силоксановых группах остальной поверхности этого образца. [54]
Как известно, поверхность окислов покрыта ионами кислорода, часть из которых образует напряженные кислородные мостики, а другая - поверхностные гидроксильные группы. Существование последних надежно установлено методами ИК-спектроскопии и ЯМР, а количество ми - / кет быть найдено по изотопному обмену с дейтерием при высокой температуре. Прогрев окислов при повышенной температуре в вакууме приводит к дегидроксилированию поверхности и сопровождается образованием координационно-ненасыщенных катионов. Окислы, содержащие ионы металлов переменной валентности, могут в этих условиях частично восстанавливаться. В атмосфере углеводородов процесс восстановления обычно проходит достаточно глубоко, приводя в пределе к образованию новой фазы восстановленного окисла. [55]
Для практического использования силикагелей определяющее значение имеет режим их регенерации. Состояние поверхности, обеспечивающее высокую поглотительную способность силикагелей по полярным веществам, и в частности по воде, сохраняется только, если регенерация проводится при температуре ниже 200 С. Проведение регенерации при температуре выше - 200 С может вызвать дегидроксилирование поверхности силикагеля и уменьшение его адсорбционной активности по воде. [56]
При дегидроксилировании поверхности чистого образца аэро-силогеля образуются силоксановые группы, не способные к специфическому межмолекулярному взаимодействию с тетрагидрофураном или триэтиламином. Теплота адсорбции на дегидроксилированной поверхности чистого кремнезема соответствует энергии песпецифического взаимодействия триэтиламина с этой поверхностью. Если же образец аэросилогеля содержит примесь А1, то при дегидроксилировании поверхности при 1100 С, наряду с образованием силоксановых групп, обнажается большое количество электроноакцепторных центров Льюиса, на которых молекулы триэтиламина хемосорбируются с выделением - 210 кДж / моль. Только после заполнения всех таких центров, доступных для молекул тетрагидрофурана или триэтиламина, теплота адсорбции резко падает до теплоты неспецифической адсорбции на силоксановых группах остальной поверхности этого образца. Таким образом, для триэтиламина, например, проявляются в основном три типа взаимодействия с разными энергиями; самая высокая из них ( - 210 кДж / моль) обусловлена хемосорбцией на примесных акцепторных центрах, энергия - 85 кДж / моль - специфической молекулярной адсорбцией на сила-нольных группах поверхности кремнезема с образованием сильной водородной связи и, наконец, энергия - 42 кДж / моль - неспецифической адсорбцией на силоксановых группах. [57]
Страницы: 1 2 3 4